
上個月有個客戶打來,說他的細胞這兩週長得越來越慢,培養基顏色偏紫——典型的 pH 偏鹼。我們請他檢查 CO₂ 感測器,果然是 TC 感測器飄掉了,實際箱內 CO₂ 濃度只剩 3% 出頭。
CO₂ 培養箱看起來就是一個恆溫箱加上 CO₂ 控制,但魔鬼全在細節裡:感測器的類型決定了開門後多快能穩回來、加熱方式影響溫度均勻性和停電耐受力、去汙方式決定你多久得跟污染搏鬥一次。選對 CO₂ 培養箱、用對方法,細胞培養的成功率和可重複性會有明顯差距。
這篇 CO₂ 培養箱完整指南把原理、感測技術、加熱方式、去汙方法、選型邏輯、污染防治、日常維護、和各類培養箱差異全部整理在一起——希望幫你在採購和日常管理上都能有具體的判斷依據。
一、CO₂ 培養箱原理:為什麼細胞培養需要 CO₂
CO₂ 培養箱的核心原理建立在培養基的 pH 緩衝化學上。搞清楚原理,後面的選型邏輯才會通。
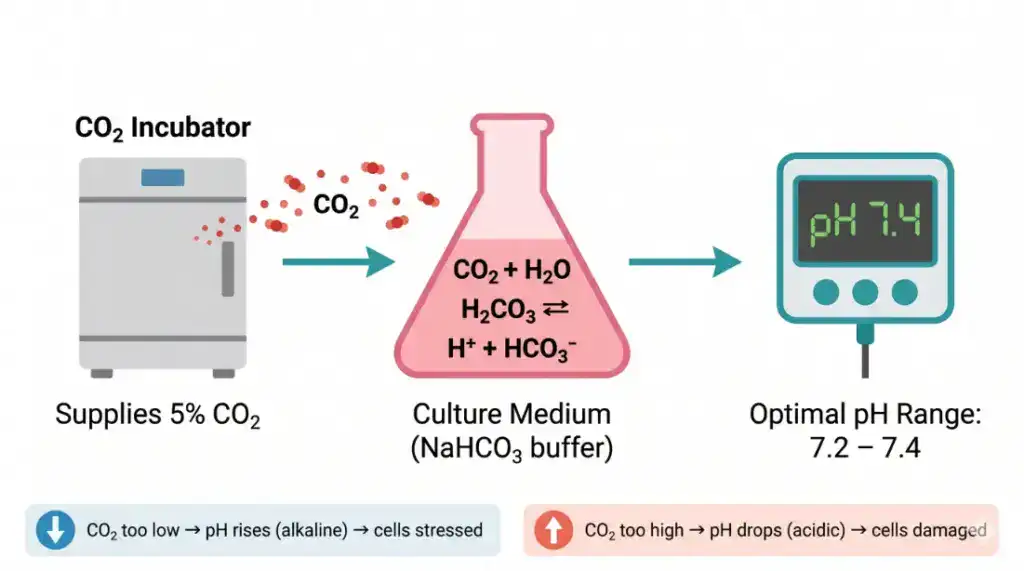
多數哺乳動物細胞的培養基用碳酸氫鈉(NaHCO₃)當 pH 緩衝系統。在這個系統裡,溶解的 CO₂ 和碳酸氫鈉形成化學平衡,把培養基的 pH 維持在 7.2–7.4 的生理範圍。如果環境 CO₂ 濃度偏低,碳酸氫鈉會分解釋出 CO₂,pH 就會升高(鹼化)——培養基變紫就是這個原因。反過來,CO₂ 太高則 pH 偏低(酸化),培養基變黃。
所以 CO₂ 培養箱必須維持穩定的 CO₂ 濃度(通常 5%),才能讓 pH 保持在細胞喜歡的甜蜜點。
用 HEPES 等非 CO₂ 依賴性緩衝液的培養基,對 CO₂ 的敏感度較低,但大多數標準培養方案還是以 NaHCO₃ + 5% CO₂ 為基礎。
二、CO₂ 培養箱控制的四大環境參數
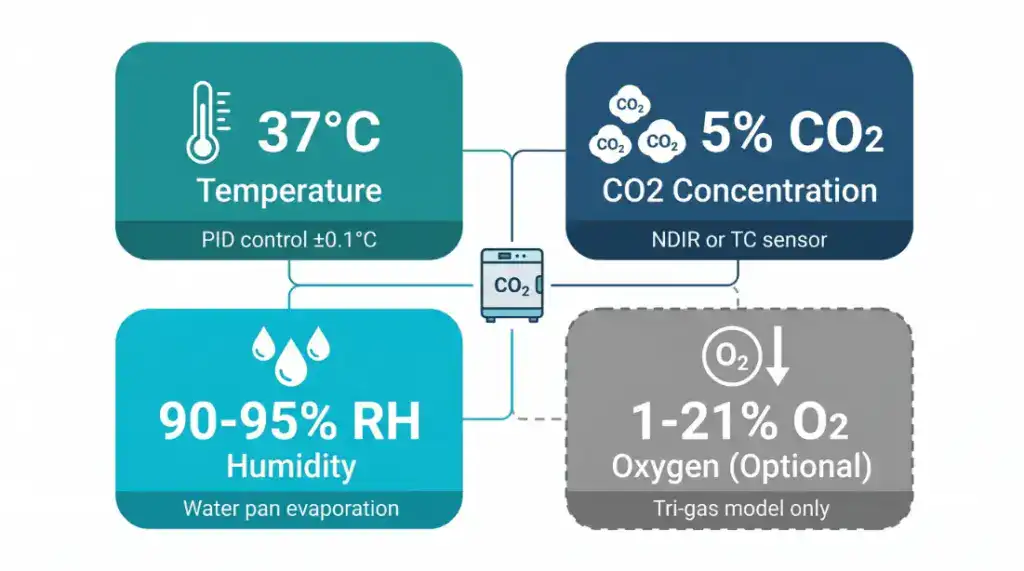
CO₂ 培養箱同時控制四個環境參數,每一個都會影響細胞的生長狀態。
溫度:標準設定 37°C,模擬人體核心體溫。控溫用 PID 控制,搭配多區域加熱(門加熱、外壁加熱)消除冷點和凝露。好的機型控溫精度在 ±0.1–0.3°C。
CO₂ 濃度:標準 5%,依培養基配方調整。透過感測器即時監測,自動調節進氣量。感測器的類型是影響開門後回穩速度和長期穩定性的關鍵差異——這個下一章會專門講。
濕度:維持在 90%–95% RH,防止培養基蒸發。主流做法是水盤被動加濕——箱底放一盤無菌蒸餾水,靠箱內溫度自然蒸發。部分機型有主動蒸汽加濕系統,開門後回穩更快。
O₂ 濃度(選配):標準 CO₂ 培養箱的氧濃度就是大氣值(約 21%)。如果你的研究需要模擬低氧環境——像腫瘤微環境研究、幹細胞低氧培養——就需要三氣體培養箱(Tri-gas Incubator),可以通入 N₂ 把 O₂ 降到 1%–20% 的任意值。
這四個參數彼此牽動:CO₂ 濃度受溫濕度影響、濕度的維持靠溫度、O₂ 控制需要 N₂ 補入又會稀釋 CO₂——選型時不能只看單一規格,要看整個控制系統的協調能力。
三、CO₂ 培養箱感測器:TC 與 NDIR(IR)的關鍵差異
CO₂ 感測器是 CO₂ 培養箱裡最核心的零件之一,直接影響日常使用體驗。選錯感測器類型,你每天都在跟 CO₂ 波動搏鬥。
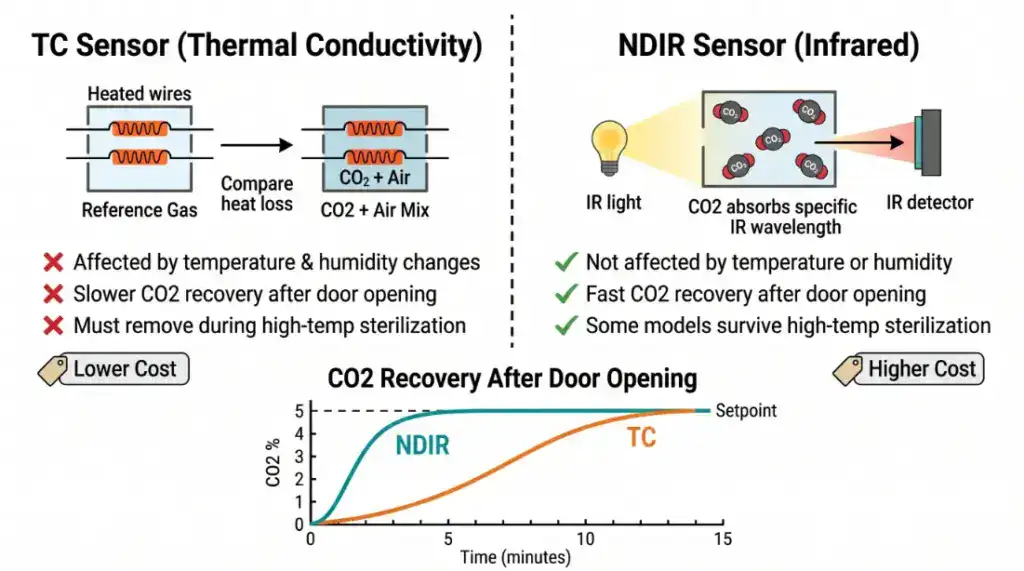
熱導式感測器(TC):靠比較 CO₂ 混合氣和參考氣體的熱傳導率差異來推算濃度。成本較低,但量測值會受溫度和濕度變化影響。開門之後箱內溫濕度劇烈波動,TC 感測器的讀值會暫時失準,需要比較長的時間才能回到正確值。而且 TC 感測器在高溫滅菌(140–180°C)的時候必須取出,不然會永久損壞。
紅外線感測器(NDIR / IR):利用 CO₂ 分子對特定波長紅外光的吸收特性來直接量測濃度。不受溫濕度變化影響,開門後的回穩速度顯著快於 TC。部分 NDIR 感測器可以在高溫滅菌時留在箱內(看廠商設計)。缺點就是價格較高。
你有沒有遇過這種狀況:早上來開培養箱拿細胞,隔壁的人中午也開了一次,下午你再開一次——每次開門 CO₂ 都要重新穩定。如果是 TC 感測器,每次回穩都要更久,細胞一整天都在承受 pH 波動。NDIR 在這種多人共用的場景下,差異非常明顯。
結論:預算允許的話,NDIR 幾乎是必選。多人共用、幹細胞、初代細胞培養這些對環境穩定性要求高的場景,NDIR 不是「加分項」,是必要配置。
選型建議:如果你現在用的 CO₂ 培養箱是 TC 機型,而且 CO₂ 波動的問題一直反覆出現,不要再花時間調校了——直接評估換 NDIR 機型的成本。長期下來省掉的校正時間和細胞損失,通常比價差更值得。
四、CO₂ 培養箱加熱方式:水套式與氣套式比較
CO₂ 培養箱的加熱方式分水套式和氣套式兩大類,選擇邏輯影響的不只是單次採購,還有後續的維護便利和停電耐受度。
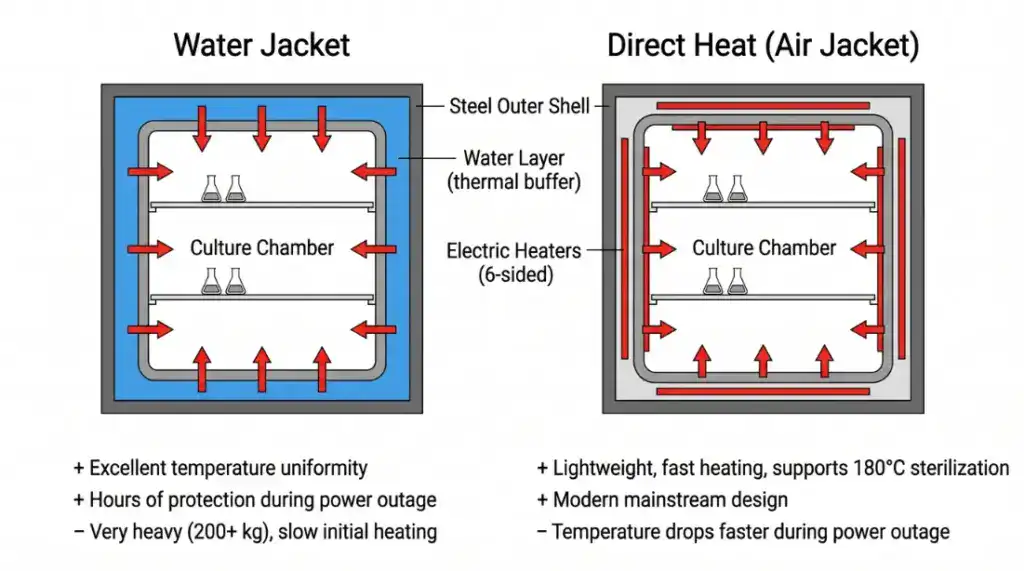
水套式(Water Jacket):箱體外殼和內壁之間灌水當熱緩衝。溫度均勻性很好,停電的時候水的大熱容量可以撐住箱內溫度好幾個小時。但設備重——灌水之後可以到 200 kg 以上,不好移動。首次加溫慢,水套萬一漏了也很麻煩。
氣套式 / 直熱式(Direct Heat):用電熱片直接加熱箱壁。設備輕、加溫快,而且可以支援高溫滅菌(不用先排水)。缺點是停電後降溫比較快。但現代高階氣套式用六面加熱加上多區域 PID 控制,溫度均勻性已經跟水套式差不多了。
現在的市場趨勢是氣套式。特別是需要高溫滅菌功能的機型幾乎都是氣套設計。如果你擔心停電問題,幫氣套式配一台 UPS 就解決了——比搬一台 200 公斤的水套式實在得多。實驗室電力配置和 UPS 選型可參閱實驗室電力系統與接地設計。
五、CO₂ 培養箱去汙方式:四種方法比較
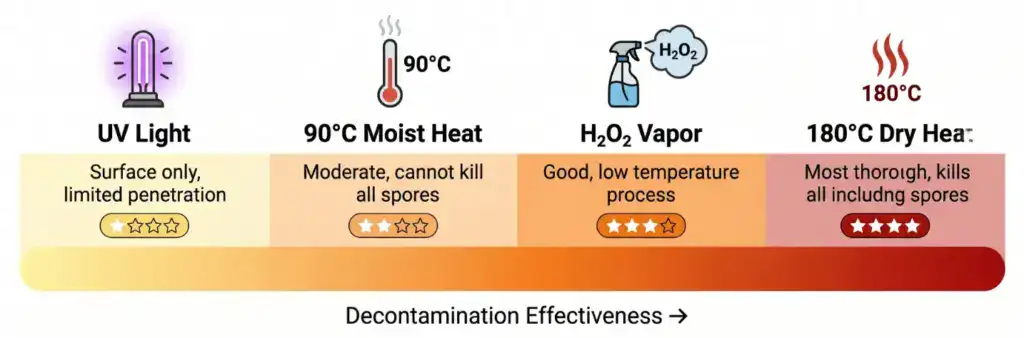
CO₂ 培養箱裡高溫高濕,是微生物的天堂。去汙能力決定了你多久得跟污染打一次仗。市面上常見的 CO₂ 培養箱去汙方式有四種:
高溫乾熱滅菌(140–180°C):最徹底的方式。箱內升到 140–180°C 維持數小時,連細菌芽孢都殺得掉。全自動執行,結束後自動降溫。只有氣套式機型才做得到(水套式溫度上不去)。滅菌前要移出所有培養物和水盤的水,也要確認 NDIR 感測器是否可以留在箱內。
紫外線(UV):部分機型箱內有 UV 燈。但 UV 穿透力有限,只對直接照射到的表面有效——層架背面、角落、管路裡面的微生物照不到。不能當唯一的去汙手段,頂多是輔助。
過氧化氫(H₂O₂)蒸汽:操作溫度低(室溫到 50°C),對不耐高溫的零件比較友善。但需要額外的 H₂O₂ 供應模組,去汙後也要充分通風排除殘留。
90°C 濕熱:效果介於 UV 和高溫乾熱之間,但不能保證殺掉所有芽孢。
我們的建議是:如果預算和機型允許,選有高溫乾熱滅菌功能的 CO₂ 培養箱。一季做一次全面滅菌,心裡踏實很多。
六、CO₂ 培養箱箱內 HEPA 與內壁材質選配
CO₂ 培養箱的箱內 HEPA 過濾和內壁材質這兩個選配項目,加價不算少,但對某些場景確實有意義。
艙內 HEPA / ULPA 過濾
部分中高階機型在箱內裝 HEPA 或 ULPA 過濾器,持續循環過濾空氣中的懸浮微粒(包括微生物)。主要好處是開門後微粒恢復速度快——幾分鐘內可以回到 ISO Class 5 等級。
多人共用或頻繁開門的場景,這個功能有實際價值。如果是你一個人專用、一天開不了幾次門,就不一定要花這筆錢。
內壁材質
不鏽鋼(SUS 304):最常見,耐腐蝕、好清潔、撐得住高溫滅菌。
電解拋光不鏽鋼:表面更滑,微生物更難附著,清潔更容易。
銅合金內壁:銅有天然的接觸殺菌效應,可以持續抑制細菌和真菌在箱壁上生長。部分廠商提供全銅內壁或銅合金層架。缺點是銅在高濕度環境中可能氧化變色(不影響功能),成本也較高。
銅合金是個不錯的加分項,但不是必要條件。做好無菌操作和定期去汙,比靠內壁材質抑菌重要得多。
七、CO₂ 培養箱六大應用場景
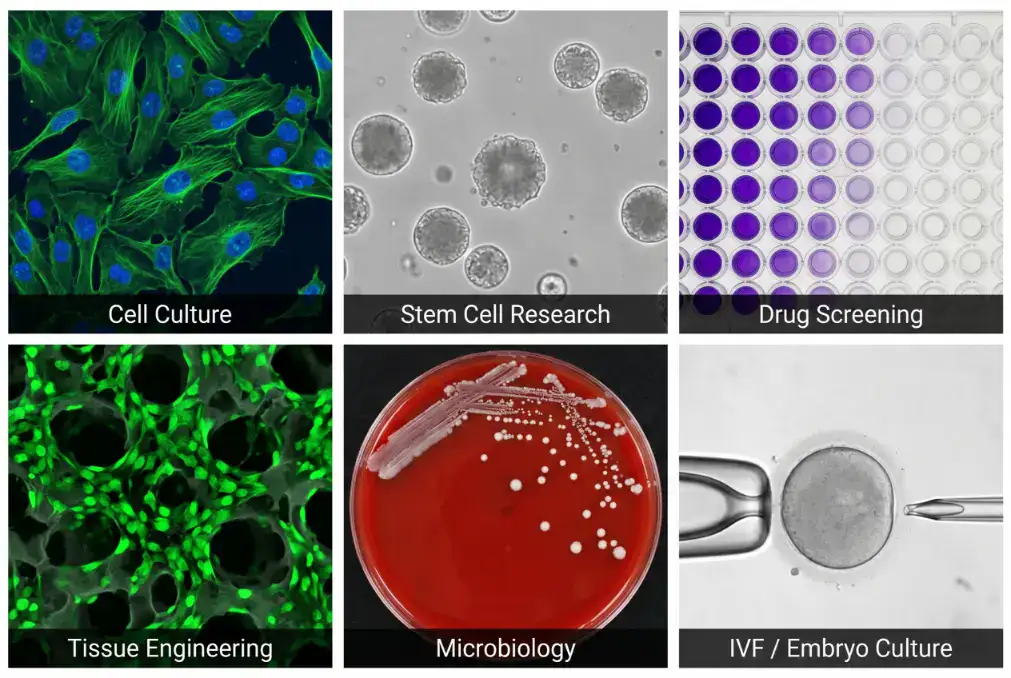
CO₂ 培養箱的應用範圍從一般細胞培養到 IVF 都有,不同場景對設備規格的要求差很多。
哺乳動物細胞培養:最核心、最廣泛的應用。建立細胞株的繼代培養、初代細胞的分離與擴增、轉染和基因編輯後的篩選擴增。標準條件:37°C、5% CO₂、≥90% RH。
幹細胞研究:ESC、iPSC、MSC 的維持和分化。幹細胞對環境波動極為敏感,建議選 NDIR 感測器、氣套式六面加熱加上艙內 HEPA 的機型。需要低氧誘導分化的話,得搭配三氣體培養箱。
腫瘤生物學與藥物篩選:腫瘤細胞體外培養、藥物毒理測試、IC50 測定。模擬腫瘤微環境的低氧條件需要三氣體培養箱。
組織工程與再生醫學:三維支架上的細胞培養、類器官培養、組織切片體外維持。這類應用通常得養好幾週甚至好幾個月,對設備穩定性和防污染能力的要求極高。
特定微生物培養:需要高 CO₂ 環境的菌種——淋病奈瑟氏菌、腦膜炎奈瑟氏菌、幽門螺旋桿菌這類嗜 CO₂ 菌。操作時須依循生物安全等級規範,在生物安全櫃內進行無菌操作。
IVF(體外受精)/ 胚胎培養:人類輔助生殖技術中的卵子和胚胎培養,對 pH 穩定性的要求極高。通常用專為 IVF 設計的培養箱,有更嚴格的 VOC 過濾和更精密的氣體控制。
八、CO₂ 培養箱選購指南:從需求反推規格
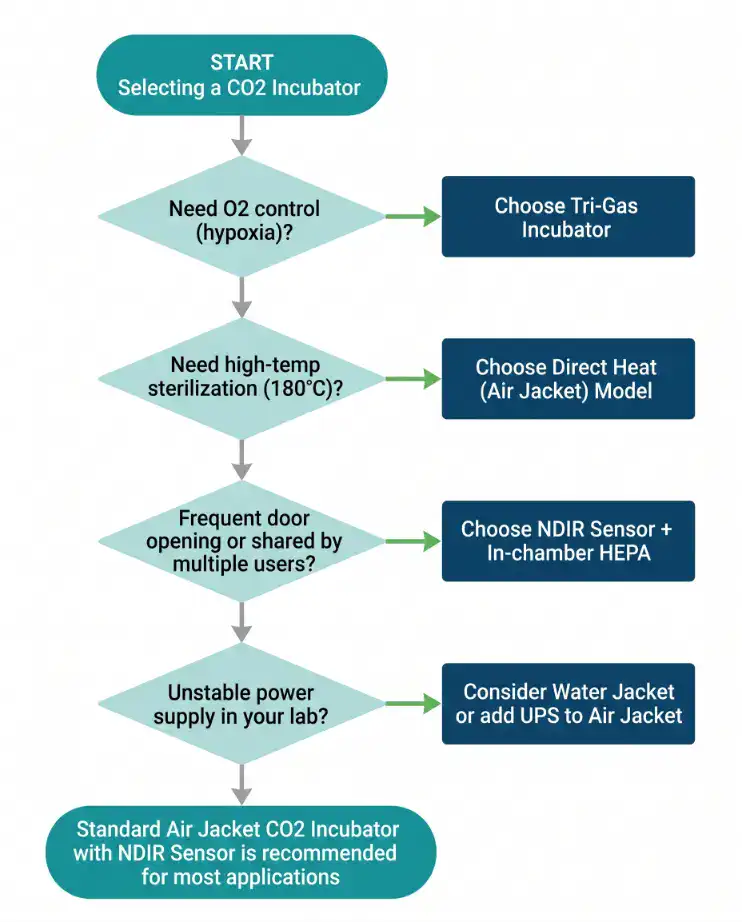
選購 CO₂ 培養箱前,先回答這幾個問題,需求釐清了規格才不會選錯。
你培養的是什麼細胞?建立細胞株、初代細胞、還是幹細胞——對環境穩定性的要求差很多。需不需要低氧控制?這決定了要不要上三氣體培養箱。多少人共用一台?開門頻率多高?這決定了 NDIR 感測器和艙內 HEPA 是不是必要的。實驗室供電穩定嗎?影響水套式和氣套式的取捨。需不需要高溫滅菌?需要的話就必須選氣套式。培養量多大?決定箱體容量。
CO₂ 培養箱容量怎麼選
CO₂ 培養箱的容量從桌上型的約 50 L 到落地型的 200 L 以上。選的時候要考慮目前的培養量加上未來 2–3 年的成長預期。寧可選略大的,也不要塞得過滿——過度裝載會影響氣流循環和溫度均勻性。
多數實驗室會配兩台以上,一來增加容量,二來一台去汙或故障的時候有備援。這個備援思維很重要——你不會想在整台 CO₂ 培養箱去汙的那三天裡,所有細胞都沒地方放。
實務觀察:只有一台 CO₂ 培養箱的實驗室,往往會因為「不敢停機去汙」而一直拖延滅菌週期,結果反而增加了污染風險。兩台輪流用、輪流去汙,才是可持續的管理模式。
規格優先順序
如果預算有限,哪些規格先顧、哪些可以先不管?按重要性排:
CO₂ 感測器(NDIR 優先)→ 去汙方式(高溫乾熱最徹底)→ 加熱方式(氣套式主流)→ 艙內 HEPA(多人共用建議有)→ 內壁材質(銅合金加分)→ O₂ 控制(視需求)→ 資料記錄與遠端監控(GMP 環境需要)
別忘了算總持有成本(TCO)
CO₂ 培養箱的設備價格只是開頭。後面還有 CO₂ 氣體消耗(箱體氣密性越好,耗氣越少)、HEPA 濾網更換、感測器校正費用、水盤用水(建議用高純度蒸餾水或去離子水)、電力消耗,以及售後服務和維修零件的供應是否方便。實驗室用水分級和氣體配管的完整內容,可進一步參閱實驗室供排水與氣體配管指南。
九、CO₂ 培養箱污染防治:日常管理的核心
污染是細胞培養中最頭痛的問題,沒有之一。CO₂ 培養箱的高溫高濕環境就是微生物的天堂——一旦污染發生,輕則單盤報廢,重則整台 CO₂ 培養箱全面去汙、所有培養物重來。
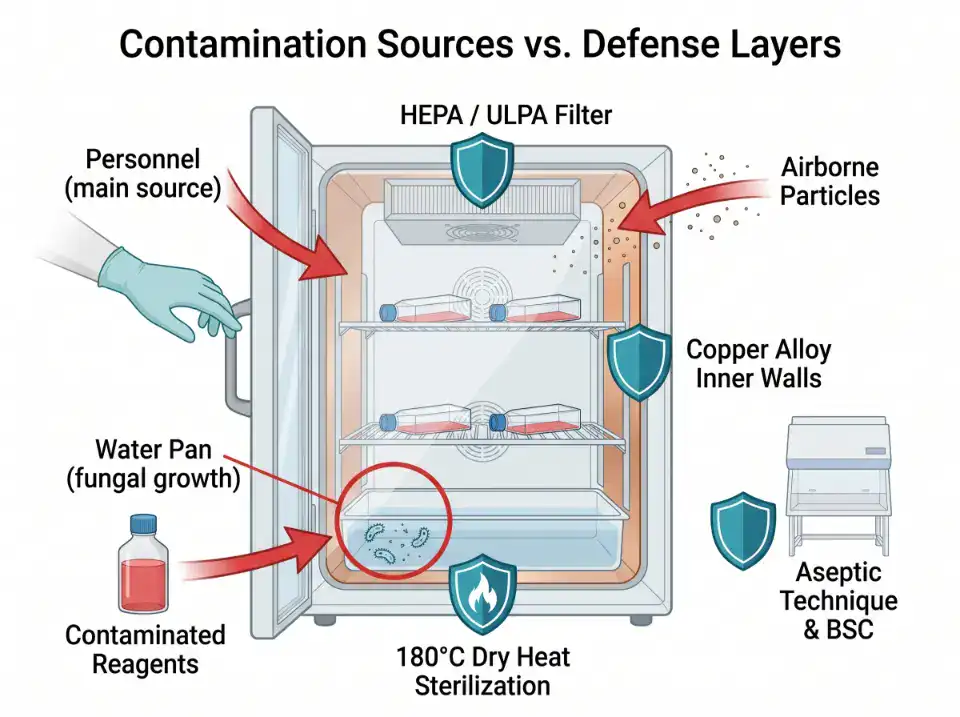
污染從哪來
人員操作:這是最主要的污染來源。開門時間太長、操作時沒有遵守無菌技術、手套或實驗衣帶入微生物。
培養基與試劑:沒有充分滅菌或已經受污染的培養基、血清、胰蛋白酶。
水盤:高溫高濕的水盤是真菌和細菌的溫床。水盤裡的水如果沒用無菌蒸餾水、或太久沒換,就會變成持續的污染源。
環境空氣:開門時外面的空氣進來,帶著灰塵和微生物。
怎麼防
無菌操作紀律是最有效、也最低成本的防治手段。所有要放進 CO₂ 培養箱的東西——培養皿、培養瓶、移液管尖端——都必須在生物安全櫃裡經過無菌處理再放入。開門時間盡量短。手套碰門把之前先用 70% 酒精擦一下。
這些聽起來很基本,但我們看過太多污染案例,追溯回去都是操作紀律的問題。設備再好,操作不到位還是會出事。
常見踩坑:水盤是最容易被忽略的污染源。我們遇過好幾次客戶反覆污染找不到原因,最後發現是水盤裡的水超過一個月沒換,長出了一層生物膜。換水這件事簡單到大家都覺得「不急」,但拖久了就會變成持續性的污染來源。
水盤管理:用無菌蒸餾水或去離子水,每 1–2 週換一次。有些人會在水裡加抑菌劑,但要確認不會影響細胞培養。最根本的做法還是定期更換。
定期去汙:即使沒有可見的污染,建議每 1–3 個月做一次全面去汙。發生已知污染事件後,必須立即清空箱內所有培養物並執行滅菌。
艙內 HEPA:持續過濾箱內空氣,降低空氣傳播的污染風險。
抗菌內壁:銅合金的接觸抑菌效果可以當防線之一,但不能當唯一的防線。
十、CO₂ 培養箱日常維護計畫
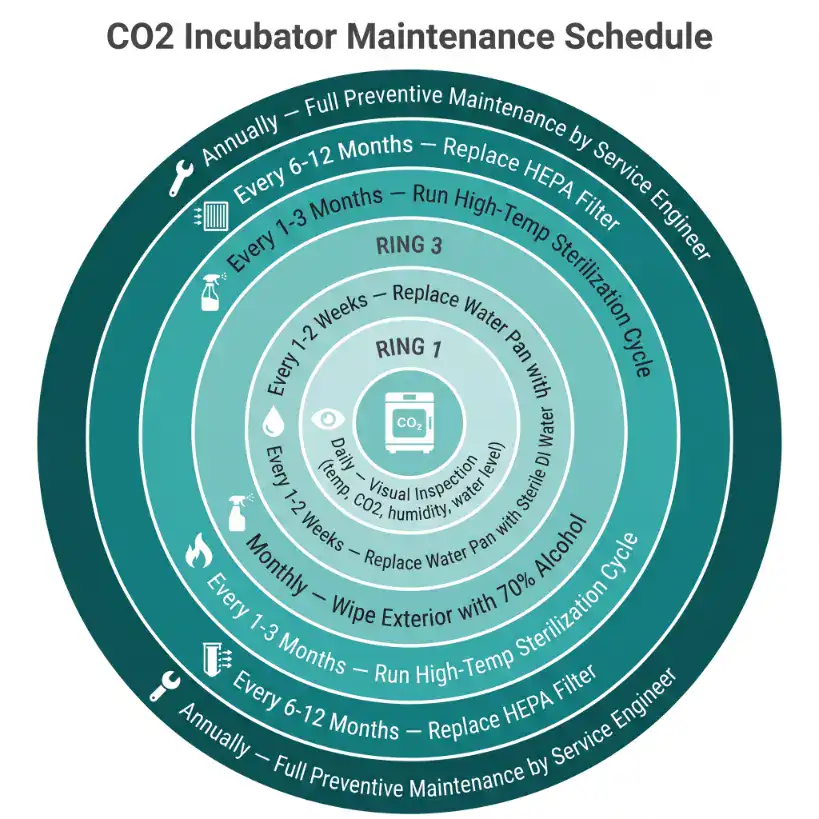
CO₂ 培養箱的長期表現取決於日常維護的落實。下面這張表建議列印出來貼在培養箱旁邊。
| 頻率 | 項目 | 說明 |
|---|---|---|
| 每日 | 目視檢查 | 確認溫度、CO₂、濕度顯示值正常;水盤水位充足 |
| 每 1–2 週 | 更換水盤用水 | 用無菌蒸餾水或去離子水,順便清洗水盤 |
| 每月 | 外部擦拭 | 70% 酒精擦門把、外殼、觀察窗 |
| 每 1–3 個月 | 內部清潔 | 取出層架和水盤,用適當清潔劑擦拭內壁,再用無菌水沖淨 |
| 每 1–3 個月 | 高溫滅菌 | 執行自動高溫去汙循環(如設備支援) |
| 每 3–6 個月 | CO₂ 感測器校正 | 依製造商建議頻率(NDIR 的校正間隔通常比 TC 長) |
| 每 6–12 個月 | HEPA 濾網更換 | 依使用環境潔淨度和製造商建議 |
| 每年 | 全面預防性維護 | 由原廠或授權服務商執行,檢查密封條、風扇、加熱元件 |
幾個容易忽略的日常細節
用水品質:水盤裡必須用高純度水(電阻率 ≥1 MΩ·cm 的蒸餾水或去離子水)。自來水含礦物質會產生水垢,含氯的水會腐蝕不鏽鋼。
開門習慣:每次開門,CO₂、溫度、濕度都會瞬間下降,外部空氣也會跑進來。建議開門前先在生物安全櫃裡把所有要放入或取出的東西準備好,一次搞定,開門時間壓到最短。
CO₂ 氣瓶管理:監控氣瓶壓力,在降到更換閾值之前及時換。建議用自動切換閥連接兩支氣瓶——一支用完自動切換到另一支,避免半夜 CO₂ 斷氣。氣體純度建議 ≥99.5%(醫療級)。
放置位置:CO₂ 培養箱要遠離門口、窗戶、空調出風口——這些地方氣流擾動大,會造成溫度波動。也要避免陽光直射,周圍留夠散熱空間。
十一、CO₂ 培養箱與其他培養箱的選型比較
「我到底該買 CO₂ 培養箱還是一般培養箱?」這是我們最常被問到的問題之一。下面這張表把五種常見培養箱的核心差異列出來:
| 比較項目 | CO₂ 培養箱 | 一般恆溫培養箱 | 低溫培養箱(BOD) | 厭氧培養箱 | 三氣體培養箱 |
|---|---|---|---|---|---|
| 溫度範圍 | 通常 RT+5 至 50°C(常用 37°C) | RT+5 至 70°C | 0–60°C(可低於室溫) | 25–45°C | RT+5 至 50°C |
| CO₂ 控制 | 有(0–20%,常用 5%) | 無 | 無 | 無(或有) | 有 |
| O₂ 控制 | 無 | 無 | 無 | 有(維持無氧) | 有(1–20%) |
| 濕度控制 | 有(90–95% RH) | 無或有限 | 無 | 有 | 有 |
| 主要應用 | 哺乳動物細胞培養 | 微生物培養、酵素反應 | BOD 測試、冷藏培養 | 厭氧菌培養 | 低氧細胞培養、幹細胞 |
| 典型價格帶 | 中高 | 低 | 中 | 高 | 最高 |
看完這張表,判斷邏輯就很清楚:
選 CO₂ 培養箱:培養哺乳動物細胞、需要維持培養基 pH 穩定(用 NaHCO₃ 緩衝系統)。
選三氣體培養箱:在 CO₂ 培養箱的基礎上,還需要控制 O₂ 濃度。三氣體培養箱本質上就是「CO₂ 培養箱 + O₂ 控制」。
選一般恆溫培養箱就夠:培養不需要 CO₂ 的微生物(大腸桿菌、酵母菌等)。不需要也不建議佔用 CO₂ 培養箱的資源。
各類培養箱的詳細比較和選型決策樹,可進一步參閱實驗室培養箱選購比較指南。

常見問題
Q:CO₂ 培養箱濃度波動很大怎麼辦? 先檢查氣瓶壓力夠不夠、管路有沒有洩漏。再看感測器是否需要校正(TC 感測器在溫濕度波動後特別容易飄)。也檢查門密封條有沒有老化、是不是有人頻繁開門。如果用 TC 感測器而且問題一直反覆,認真考慮升級到 NDIR 機型。
Q:CO₂ 培養箱箱內出現霧氣或水滴怎麼處理? 通常是濕度過高或門玻璃內外溫差大。確認水盤水量沒有過多、門加熱功能正常運作。適度降低濕度設定或擦拭觀察窗內側可以暫時改善。
Q:CO₂ 培養箱多久做一次高溫滅菌? 沒有發生已知污染的正常使用下,建議每 1–3 個月做一次。發生污染事件後必須立即清空箱內所有培養物並執行滅菌。滅菌前移出水盤的水,確認感測器是否需要取出(看機型)。
Q:CO₂ 培養箱水盤可以加抑菌劑嗎? 部分人會加硫酸銅或市售抑菌劑。用之前要確認不會揮發影響細胞,也不會腐蝕箱體。最安全的做法還是定期更換無菌蒸餾水。
Q:CO₂ 培養箱可以養細菌嗎? 可以,但僅限需要高 CO₂ 的特定菌種(淋病奈瑟氏菌等)。一般好氧菌用恆溫培養箱就行,不需要佔用 CO₂ 培養箱。
Q:CO₂ 培養箱的 TC 和 NDIR 差價值得嗎? 多人共用、初代細胞、幹細胞培養——這些場景下 NDIR 的快速回穩和不受溫濕度干擾的特性,能明顯降低 CO₂ 波動造成的細胞生長異常。從長期實驗品質的角度看,這個差價通常值得。
Q:CO₂ 培養箱停電怎麼辦? 水套式靠水的大熱容量可以撐數小時。氣套式降溫快,建議配 UPS(至少維持 30–60 分鐘)。不管哪種,停電期間不要開門。停電超過數小時,要準備把培養物轉移到有供電的培養箱。
Q:CO₂ 培養箱選購要找什麼樣的廠商? 看四件事:CO₂ 感測器(NDIR/TC)的原廠訓練資格、HEPA 與感測器校正服務的在地能力、台灣的零件庫存與維修反應速度、能不能根據你的細胞類型給型式建議(不是只推最貴的)。CO₂ 培養箱是日常運轉的核心設備,售後服務的反應時間直接影響實驗進度——找在地有完整服務團隊的代理商會差很多。
延伸閱讀
相關產品
本文由原拓科技編撰,以超過 30 年實驗室規劃與設備整合經驗為基礎,提供 CO₂ 培養箱的選型與應用參考。如需選購諮詢,歡迎與我們聯繫。
