
稽查員走進你的 QC 品管實驗室,第一眼看的不是 SOP 文件夾,是物理空間怎麼分。取樣室在哪、留樣怎麼放、化學分析跟微生物分析有沒有分開、HPLC 旁邊有沒有人在簽紙本紀錄——這些「外觀就看得出在管理」的物理線索,往往比書面文件更早影響稽查的走向。
GMP 品管實驗室跟一般化學實驗室的差別,不在於儀器多少或空間大小,而在於整套空間是依照法規、樣品流向與資料完整性的邏輯一起設計出來的。動線設計不到位,光靠 SOP 補救通常很有限;分區設計不對,後續稽查時往往要反覆解釋。所以這篇主軸放在 PIC/S GMP 西藥廠 QC 實驗室——這是繁中圈搜尋意圖最強、決策金額最高、稽查最嚴的那一類。
保健食品 GMP(衛福部食品工廠 GMP)、化妝品 GMP(化粧品優良製造準則)的品管實驗室,硬體規劃邏輯有八成相通——動線、分區、儀器配置都可以直接參考本文,差別主要在法規依據、留樣要求與稽查單位。保健食品與化妝品 GMP 的產業特殊需求未來會有專文補充;現階段三產業適用的對照表,文末 FAQ 有完整版本。
適用範圍聲明:本文主要討論台灣西藥製造廠的 GMP QC 品管實驗室規劃,並以 PIC/S GMP、TFDA 公告版本與常見藥廠稽查實務為基礎。不同產品類型——例如無菌製劑、原料藥、生物製劑、高活性藥物、保健食品與化妝品——其空間、潔淨度、HVAC 與驗證要求可能不同,實際規劃仍應依產品風險、製程特性與主管機關要求進行評估。本文中的數值與時程屬於常見規劃起點,不是固定規格。
一、GMP 品管實驗室與一般化學實驗室的根本差異
很多人以為,GMP 品管實驗室就是「加上幾道門禁、幾份 SOP」的化學實驗室——這個想法低估了 GMP 的滲透深度。GMP 不是疊在化學實驗室上面的「合規層」,而是從第一天的平面圖就要重新思考整套空間邏輯的不同物種。
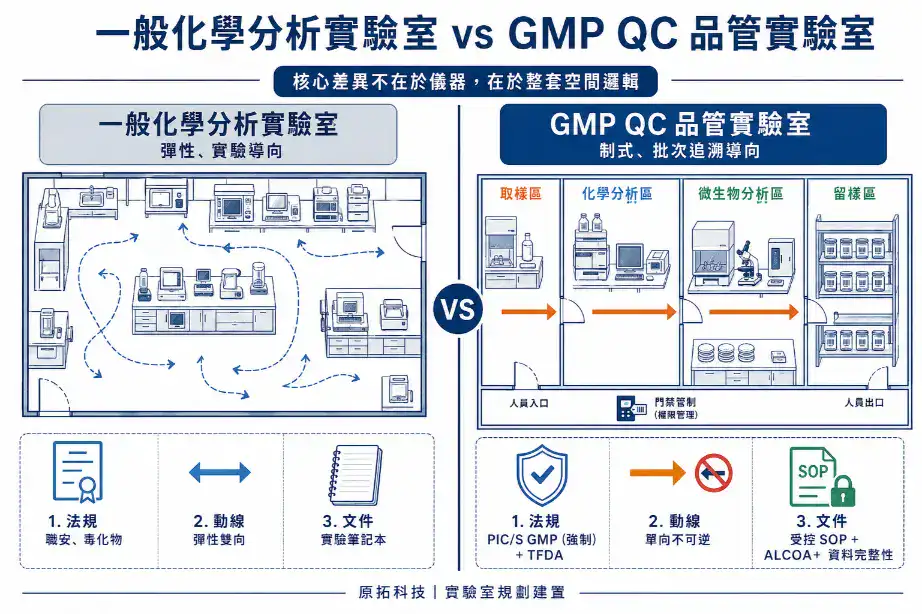
差別來自三個層次。
法規驅動,不是設備驅動
一般化學實驗室規劃時,最常見的起點是「我們要買哪些儀器」「需要幾個排煙櫃」「桌面要多大」。設備清單先列出來,空間配置再套上去。GMP 品管實驗室不是這樣——它的起點是**「PIC/S GMP 第六章對 QC 實驗室規定了什麼」**。法規規定了取樣、留樣、文件、稽查路徑的物理邏輯,設備配置反而是後面才確定。
這個順序顛倒了,整個專案的決策節奏就不一樣。一般實驗室的需求訪談會先問實驗種類;GMP QC 實驗室的需求訪談會先問產品線、批次數、稽查頻率、客戶端額外要求。
樣品流向是制式單向管理,不是污染防護邏輯
一般化學實驗室和生技 R&D 實驗室規劃動線時,主要邏輯通常是「污染防護」——人員淨化、廢棄物分流、潔淨梯度。GMP QC 實驗室也有這些,但它有一個更高優先的考量:樣品從取樣到留樣的流向應採單向管理,每個階段的狀態清楚、轉換受控。
取樣後的樣品要有清楚的接收與登錄流程;分析中的樣品不應跟留樣混在一起;留樣的取用要有 SOP 授權與紀錄。這個邏輯來自 GMP 的批次追溯思維——每一批產品從原料、製程到成品,都要能在文件上追到任一時間點的位置和狀態。空間設計如果讓樣品有「可以隨意繞回去」的物理通道,就會讓稽查員懷疑追溯邏輯的執行強度。
這不代表樣品「永遠不能往回走」。實務上,OOS/OOT 調查、複驗、客訴處理、安定性追蹤、主管機關抽驗等情境,都可能需要從留樣或前一階段重新取用樣品。重點不是「禁止取用」,而是取用要有授權、有紀錄、有偏差或調查邏輯支持。空間規劃的責任,是讓「正常工作流」順暢、讓「例外處理」也有受控的物理路徑可走。
這跟 C1 生技醫藥研發實驗室的污染防護思維有不同的重心——研發實驗室的樣品流動較有彈性,依實驗需要調整;QC 實驗室的樣品流動則是有狀態紀錄、有時間戳記的,每個動作都會進入批次紀錄。
文件導向,每個動作都要有紙本或電子留痕
一般實驗室的研究員做完實驗,記錄寫在筆記本或 Excel;GMP QC 的分析人員做完分析,記錄要進入受控文件系統(LIMS 或紙本受控表單),有獨立簽核、時間戳記、變更追蹤。這意味著每台儀器旁邊要有紀錄空間,每個分析步驟要有簽名動線,每份報告要有獨立審核流程。
這些需求會直接反映在空間配置上。你不能讓 HPLC 旁邊只有一張小到放不下記錄本的桌子;你不能讓微生物實驗室跟化學分析實驗室共用一個簽名站。文件導向意味著空間裡有相當比例(通常 15–25%)是給「紀錄與審核」用的,不是給做實驗用的。
一張表看懂兩者差異
| 比較項目 | 一般化學分析實驗室 | GMP QC 品管實驗室 |
|---|---|---|
| 法規依據 | 職安、毒化物、ISO 17025(選擇性) | PIC/S GMP(強制)、TFDA、ICH Q7/Q10、21 CFR Part 11 |
| 動線邏輯 | 污染防護(分區、潔淨梯度) | 樣品單向管理(受控狀態轉換)+ 污染防護 |
| 空間分區 | 依實驗類型彈性 | 依 GMP 流程制式分區(取樣 / 接收 / 準備 / 化學 / 微生物 / 留樣 / 文件) |
| 設備驗證 | 出廠校驗、定期校正 | IQ / OQ / PQ 三階段驗證 + 定期再驗證 |
| 文件要求 | 實驗記錄本 | 受控 SOP、批次紀錄、ALCOA+ 資料完整性 |
| 樣品追溯 | 樣品標籤即可 | 完整批次追溯,從取樣到銷毀皆有文件 |
| 稽查頻率 | 不定期 | 定期 + 不定期(依主管機關風險評估、產品類型、歷史缺失與外銷市場要求而定) |
| 人員資格 | 學歷+經驗 | 學歷+經驗+受過 GMP 訓練+品保紀錄 |
最重要的結論:GMP QC 實驗室不能用一般化學實驗室的規劃思維「升級」上去,建議從一開始就用 GMP 邏輯設計。如果你正在改建既有的化學實驗室成為 QC 實驗室,要做的不是加裝幾道門禁,而是重新檢視整套動線是否符合樣品單向管理邏輯。
常見踩坑:很多廠在第一次規劃時,把 QC 實驗室當成「研發實驗室加上更嚴格的 SOP」,動線、分區都沒重新設計。等第一次稽查走進來,發現取樣後的樣品要穿過化學分析區才能到留樣室——這個動線錯誤無法用 SOP 補救,只能重新隔間或重新拉走道。實務上,等到稽查缺失後才補救的改建成本,常會顯著高於前期規劃成本;尤其涉及隔間、HVAC、壓差與再驗證時,達前期規劃成本的數倍並不罕見,但實際金額仍須依個案專案條件評估。
二、PIC/S GMP 與台灣 TFDA 法規框架
寫到法規這段,最容易踩的地雷是把不同層級、不同年代、不同適用對象的規範混在一起講。所以這節我會盡量分清楚:哪些是法規強制、哪些是業界慣例、哪些是國際建議。
PIC/S GMP 在台灣的法定地位
PIC/S 全名是「國際醫藥品稽查協約組織」(Pharmaceutical Inspection Co-operation Scheme),由各國 GMP 稽查權責機關組成,是目前全球規模最大的 GMP 標準協合組織,目前有 56 個會員國。台灣的衛生福利部食品藥物管理署於 2013 年(民國 102 年)1 月 1 日正式成為第 43 個官方參與機構。
台灣西藥 GMP 的法規依據是《藥物優良製造準則》與衛福部公告的「西藥藥品優良製造規範」。其中「西藥藥品優良製造規範」參照 PIC/S GMP 架構,由衛福部以中英文對照公告,並明確標示適用日期。所以對台灣的西藥廠來說,正式的法規文本是衛福部公告版本,PIC/S 原文則作為解讀、附則查詢、國際對接的參考。
實務規劃時的兩個原則:
- 以 TFDA/衛福部公告版本與適用日期為準,不是直接拿 PIC/S 英文版當唯一法規文本
- 涉及 PIC/S 附則(Annex 1 無菌製劑、Annex 11 電腦化系統等)或最新國際趨勢時,搭配 PIC/S 原文與相關指引解讀
當 PIC/S 國際組織更新條文時,衛福部會配合更新並公告週知。寫 SOP、做廠房設計時,要看的是衛福部最新公告版本,不是早期英文原文版——因為衛福部公告版本會標示生效日期,舊版本可能已不適用。
PIC/S GMP 對 QC 實驗室最相關的兩個章節
整本 PIC/S GMP 第一部(Part I)共九章。對 QC 實驗室規劃影響最大的是第三章「廠房設施與設備」和第六章「品質管制」。
第三章規範了廠房整體設施,包括:
- 廠房應有足夠空間,避免混淆和交叉污染
- 廠房應依生產流程作有秩序之安排
- 設備之設計、位置與安裝,應便於操作、清潔和維護
- 品質管制實驗室通常應與生產區域隔離,特別是用於儀器分析、生物試驗、微生物試驗及放射性同位素操作的實驗室,更應彼此分隔
最後一條是 QC 實驗室分區設計的法規依據——化學分析、微生物試驗應彼此分隔不是業界慣例,是法規要求。
第六章規範品質管制本身,包括:
- 品質管制部門的職責、組織與獨立性
- 良好品質管制實驗室規範(GLP 概念)
- 取樣的人員資格、方法、記錄
- 試驗的執行、記錄、報告
- 保留樣品的種類、數量、儲存條件、保留期間
- 安定性試驗計畫
第六章是 QC 實驗室「在做什麼」的法規定義,第三章是「應該長什麼樣」的物理規範。兩章一起看,才能把空間配置跟法規要求對齊。
TFDA、ICH 與 21 CFR 的補充角色
衛福部食藥署除了採用 PIC/S GMP 作為西藥規範本身,還會發布補充指引——例如查廠注意事項、缺失改善公告、特定劑型的補充規範。撰寫 SOP 時這些補充文件也要納入。
ICH(International Council for Harmonisation)是國際藥品法規協合會議的縮寫,發布的指引中,**ICH Q7(API GMP)**和 **ICH Q10(藥品品質系統)**對 QC 實驗室規劃影響最直接。Q7 規範原料藥的 GMP,包括 QC 部分;Q10 是更高層次的「整體品質系統」框架,把 QC、QA、生產整合成一個有機系統。
21 CFR Part 11 是美國 FDA 對電子紀錄與電子簽名的規範。對台灣的 GMP 廠來說,21 CFR Part 11 不是台灣法規強制——但若同時滿足兩個條件「使用電子紀錄/電子簽名」+「產品受 FDA 管轄(外銷美國或對美申請)」,就應該納入 Part 11 評估。對使用 LIMS、電子實驗筆記本(ELN)的 QC 實驗室來說,這部分規範會直接影響系統選型和空間配置(電子簽核站、稽核軌跡、權限管理)。如果只用紙本紀錄,Part 11 的適用範圍就有限。
資料完整性:ALCOA+ 是底線
資料完整性(Data Integrity)是 PIC/S 最近十年稽查重點之一。FDA 從 2015 年起,與資料完整性相關的警告函(Warning Letter)數量大幅增加;PIC/S 在 2021 年發布 PI 041-1「Good Practices for Data Management and Integrity in Regulated GMP/GDP Environments」,把資料完整性的要求系統化。
主要原則叫做 ALCOA+——Attributable(可歸屬,誰做的查得到)、Legible(清晰可讀)、Contemporaneous(即時記錄,不是事後補)、Original(原始資料或經查證的副本)、Accurate(準確),加上 Complete(完整)、Consistent(一致)、Enduring(持久保存)、Available(可取得)共 9 個原則。歐盟 GMP 規範近年正擴充為加入 Traceable 第 10 原則的 ALCOA++,但截至本文撰寫時,ALCOA+ 仍是 PIC/S 主要採用的版本,台灣 GMP 廠以此為實務基準即可。
ALCOA+ 除了文件層面的要求,也有物理空間規劃面向。要做到 Contemporaneous(即時記錄),代表每台儀器旁邊都要有書寫或電子記錄空間;要做到 Attributable(可歸屬),代表每個實驗工位都要能識別個人身分(不是共用帳號);要做到 Original(原始資料),代表紙本與電子記錄的儲存空間要受控、不能在普通儲物櫃。
法規層級分清楚:強制 vs 慣例 vs 建議
寫到這裡,把三種規範的層級整理清楚,避免誤把建議當強制:
| 規範 | 層級 | 適用對象 | 不遵守的後果 |
|---|---|---|---|
| PIC/S GMP(衛福部公告版本) | 法規強制 | 台灣西藥製造廠 | 無法取得 / 維持 GMP 認證、無法製造 |
| TFDA 補充指引、查廠注意事項 | 法規強制 | 台灣西藥製造廠 | 稽查缺失、限期改善 |
| ICH Q7、Q10 | 業界共識的標準 | 國際接軌的藥廠 | 部分內容已納入 PIC/S,部分未納入;未納入部分屬於高度建議 |
| 21 CFR Part 11 | 法規強制(美國) | 外銷美國的藥廠 | 無法通過 FDA 稽查、無法外銷 |
| ALCOA+ | 建議標準(PIC/S 引用) | 全球 GMP 廠 | 稽查時資料完整性會被深入檢視 |
寫 SOP 或規劃廠房時,「必須」、「強制」、「法規要求」這些字只用在 PIC/S GMP 條文和 TFDA 公告;其他層級的規範用「業界標準」「主流做法」「建議」帶出來。把這三層分清楚,才不會被內行讀者抓到「這家不懂法規層級」。
三、QC 實驗室的核心動線:樣品單向管理是設計起點
寫到這節,我想先講一個觀念上的調整:規劃 QC 實驗室時,建議優先釐清的不是要放什麼儀器,而是樣品從哪裡進、往哪裡走、最後到哪裡留。把這條動線釐清楚,再去談分區和儀器配置,後續會順很多。
樣品的七個階段
從原物料、製程中、成品到留樣,每一個樣品在 QC 實驗室裡會經過七個階段。這七階段不是 PIC/S 條文寫的固定流程,而是業界對 QC 工作流的標準描述——把它畫成一條時間軸,就是 QC 實驗室空間規劃的骨架。
取樣 → 樣品接收 → 樣品準備 → 化學分析 / 微生物分析 → 數據處理 → 報告 → 留樣
每個階段的物理動作不同:
- 取樣:在原料倉庫、製程現場或成品倉庫進行。取樣本身常常獨立成一個空間(取樣室或 Sampling Booth),原因下一節會講
- 樣品接收:樣品送到 QC 實驗室,由樣品管理員登錄、編號、貼標,進入 LIMS 系統
- 樣品準備:稱重、稀釋、萃取、過濾——前處理階段,常會用到天平、排煙櫃、純水
- 化學分析 / 微生物分析:依檢測項目分流到對應的儀器室或微生物室
- 數據處理:分析人員在儀器旁完成原始紀錄,再到文件區做進一步審核、計算、表格製作
- 報告:QA 審核、簽核、發出 CoA(Certificate of Analysis)、批次放行
- 留樣:依規定保留期間儲存於留樣室
「狀態受控、單向管理」是主要原則
七個階段的重點除了「順序」,還包含狀態管理——每個階段的樣品都有清楚的狀態標示(待分析 / 分析中 / 已完成 / 已留樣 / 已銷毀),且狀態轉換要有授權、紀錄與物理區隔。
這個原則的物理意義是:
- 樣品接收區不能跟取樣室共用空間:避免新樣品和已登錄樣品混淆
- 樣品準備區的廢棄物不能流回樣品接收區:避免污染未處理樣品
- 已完成分析的樣品不能跟還在等待分析的樣品放在一起:避免狀態誤判
- 留樣的取用要有授權:留樣室不是「只進不出」的封閉空間——OOS/OOT 調查、複驗、客訴處理、安定性追蹤、主管機關抽驗都可能需要從留樣取出。但任何取用都應依 SOP 授權、登錄、留痕,並有偏差或調查紀錄支持,而不是任意取放
換句話說,「單向管理」講的是正常工作流的設計方向,不是「樣品永遠不能往回走」。實務上樣品因偏差調查而被重新取用的情況並不少見,重點在於:取出、使用、返庫或銷毀的每一步都要受控。
這個邏輯跟 C1 生技醫藥研發實驗室規劃指南的「污染防護」邏輯有不同的重心。研發實驗室的樣品流動較有彈性——做完細胞培養可以回去重新接種,做完 PCR 可以再跑一次,因為實驗本身就是探索性的。QC 實驗室的樣品流動則是制式、有狀態紀錄、有時間戳記的——每個動作的時間和操作者都會進入批次紀錄,即使因調查需要回頭,也是另一個受控流程,不是「順手取用」。
動線設計常見錯誤
從實務經驗看,新建 QC 實驗室或從化學實驗室改建時,最常見的動線錯誤有這幾個:
錯誤一:取樣後直接進儀器室。沒有獨立的樣品接收區,取樣的人直接拿樣品進到 HPLC 室開始檢測。這會讓樣品的「登錄、編號、簽收」步驟跟「分析」混在同一個空間,文件流向亂掉。解法:樣品接收區應該獨立,至少有一個樣品登錄站(電腦 + LIMS 終端 + 樣品暫存櫃)。
錯誤二:留樣室跟樣品接收區共用走道。新到的樣品和已留存多年的樣品共用一個入口,標籤一不小心就會混淆。解法:留樣室的入口應該獨立,最好設計成「只有樣品管理員能進」的權限管制空間。
錯誤三:化學分析跟微生物分析共用人員動線。同一個分析人員上午做 HPLC、下午做微生物——本身沒問題,但如果空間設計沒有換鞋、洗手、換袍的緩衝區,微生物的污染風險會跟著進到化學區。解法:化學區和微生物區之間要有緩衝區,至少有洗手台和工作服更換空間。
錯誤四:留樣室空間第一年就規劃剛剛好。沒有預留未來三年的擴充空間,第二年就爆滿,只能在普通儲存櫃裡塞留樣,破壞了留樣室的環境控制和追溯邏輯。解法:留樣室空間至少預留 30–50% 的擴充冗餘(這部分第六章會詳細談)。
實務觀察:很多廠在第一次稽查時被指出「動線不順」,第一反應是「我們的 SOP 規定樣品要這樣走」。但稽查員看的不是 SOP 寫什麼,是物理空間有沒有支持這個流向。如果空間配置讓「樣品繞回去」變得容易,稽查員會合理懷疑 SOP 的執行強度。良好的動線設計應盡量透過物理配置降低誤操作機率,而不是完全依賴人員記憶 SOP。
四、QC 實驗室的功能分區設計
樣品動線講完了,下一步是把動線轉換成空間分區。QC 實驗室的功能分區不是「把房間切成幾塊」這麼簡單,而是讓每個分區的物理特性(潔淨度、溫濕度、壓差、人員權限)符合該階段的工作需求。
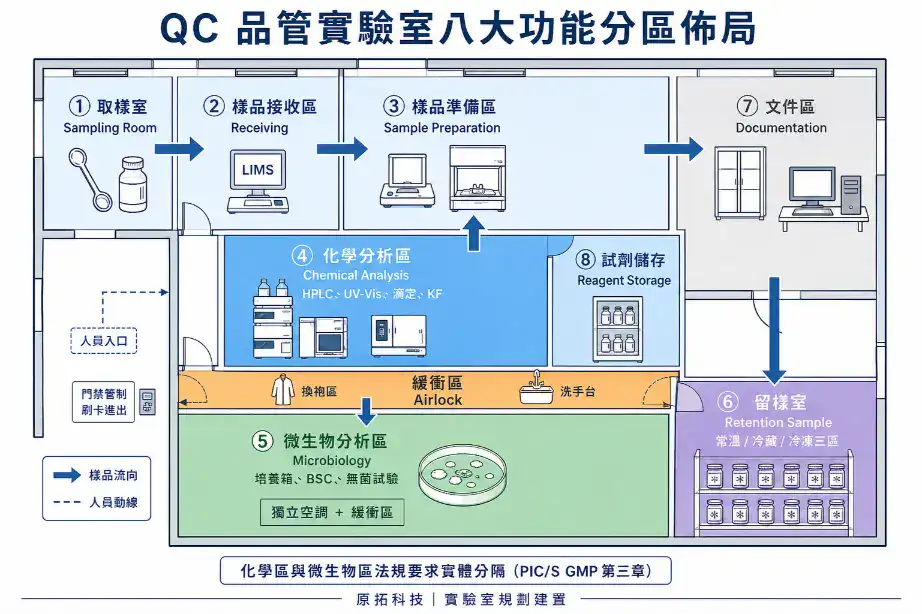
八大功能區
QC 實驗室的標準功能分區可以分成八個。不同規模的廠不一定都會有獨立空間,但每個功能至少要在規劃上被識別出來,不能默認用同一個房間 cover 所有需求。
| 分區 | 主要工作 | 環境需求 | 人員權限 |
|---|---|---|---|
| 取樣室 | 從原料/製程/成品取樣 | 局部潔淨(依產品而異) | 取樣人員 |
| 樣品接收區 | 登錄、編號、貼標、暫存 | 一般環境,受控進出 | 樣品管理員 |
| 樣品準備區 | 稱重、稀釋、萃取、過濾 | 通風、純水供應、排煙櫃 | 分析人員 |
| 化學分析區(儀器室) | HPLC、GC、UV-Vis、IR | 溫濕度控制、防震、UPS | 分析人員 |
| 微生物分析區 | 計數、鑑定、無菌測試 | 潔淨度(部分需 BSL-2) | 微生物分析人員 |
| 留樣室 | 保留樣品儲存 | 常溫 / 冷藏 / 冷凍 | 樣品管理員 |
| 文件區 | 紙本紀錄、SOP、報告審核 | 一般環境,文件儲存櫃 | 全部 QC 人員 |
| 試劑 / 標準品儲存 | 試劑、標準品、參考物質 | 常溫 / 冷藏 / 避光 | 分析人員 |
化學區與微生物區的分隔設計
PIC/S GMP 第三章要求儀器分析、生物試驗、微生物試驗應彼此分隔——這是法規層面的「分隔」要求,不是工程細節的指定。
「分隔」的法規意義是「實體區隔,避免交互污染」,但沒有規定一律要採用完全獨立的 HVAC 系統。實際工程做法應依風險評估決定,常見的考量包括:
- 產品特性:是否涉及無菌製劑、高活性藥物、生物製劑
- 操作型態:是否有開放式操作、揮發性溶劑、粉塵或氣膠
- 微生物項目:是否包含無菌試驗、環境監測、致病菌檢驗
- 空間規模:小型實驗室與大型多製程廠房的工程選項不同
依據風險評估結果,工程上的設計選項由弱到強大致是:
- 基本款:實體隔間 + 共用空調但有獨立排氣 + 緩衝區
- 加強款:實體隔間 + 部分區域獨立 HVAC + 壓差設計
- 完整款:完全獨立 HVAC + 壓差控制 + 人員緩衝區 + 獨立廢棄物動線
對於有揮發性溶劑、粉塵、高活性物質、無菌試驗或高污染風險的場景,強烈建議優先採用獨立或明確分區控制的 HVAC 設計,避免空氣交互污染。但不需要把所有 GMP QC 實驗室都拉到「完整款」——這個過度設計會大幅增加建置與運轉成本。
「分隔」的物理表現也包括:
- 獨立人員動線:分析人員從化學區到微生物區之間應有緩衝區(換袍、洗手、消毒)
- 獨立廢棄物動線:化學廢液和生物廢棄物的處理流程分開
- 盡量不共用儀器:天平、培養箱、移液器這類「兩邊都會用到」的儀器,常見做法是各自配置一套,避免交叉污染
實務上,小型廠房有時候會把化學區和微生物區只用「玻璃隔間」分開、沒有任何氣流分區設計。這個做法在風險低的情境下可能可以解釋,但若涉及無菌試驗或揮發性化學品,稽查時容易被質疑。設計階段先做風險評估,把工程設計層級訂清楚,比事後改建省成本。
取樣室(Sampling Booth)獨立的理由
取樣室是 QC 流程的起點,也是最常被忽略的獨立空間。很多廠把取樣放在原料倉庫的角落、用塑膠布圍出來,理由是「反正取樣動作很快」。
獨立取樣室的價值在於:
- 避免原料倉庫污染:取樣時打開原料容器,會釋放粉塵或揮發氣體;如果在開放倉庫進行,會污染倉庫內其他原料
- 避免取樣人員交叉污染樣品:開放空間的氣流不可控,取樣的同時可能引入空氣中的微粒
- 取樣紀錄的物理位置:取樣後立即在獨立空間貼標、登錄、簽核,紀錄的時效性和正確性比較高
- 稽查友善:稽查員看到獨立的取樣室,會直接認知這個廠有把取樣當成獨立工作流程,而不是順手做的雜事
取樣室通常有獨立的 HVAC、局部排氣(取易揮發或粉塵原料時)、不鏽鋼台面、可清潔的牆面。如果是高活性 API 或細胞毒性藥物(如腫瘤藥),取樣室可能需要負壓設計、手套箱或封閉式取樣設備(Sampling Port)。
可以延伸閱讀的服務細項:排氣式 PP 藥品櫃 和 鋼瓶櫃 都是取樣室常用的儲存設備,分別處理化學藥品和氣瓶。
各區的潔淨度需求
不是所有 QC 實驗室都需要 GMP 等級的潔淨空間。實務上的潔淨度需求依產品類型、檢測項目、是否涉及無菌製劑、操作開放程度而異,並應依 GMP Annex 1、廠內 SOP 和風險評估訂定,不是套用固定等級。常見的設計起點:
- 化學分析區:通常一般環境(換氣常見起點 6–10 ACH,依設備發熱與排氣需求調整)即可,不需要 ISO 等級的潔淨度
- 微生物分析區:依檢測項目和樣品風險而異
- 一般微生物限度試驗(菌數、致病菌等)不必然需要高等級潔淨室,常見做法是受控環境配合 BSC 操作即可
- 環境監測樣品的培養本身不一定要在 ISO 7 背景進行,重點在於培養箱操作環境受控、避免培養過程被污染
- 無菌試驗通常以 Annex 1 規範為基準,操作區(無菌操作)多在 ISO 5(A 級區)下進行,背景區依風險評估常見落在 ISO 7(B 級區)
- 涉及無菌製劑相關檢測或高風險開放操作時,需依 Annex 1、廠內風險評估與 SOP 規劃對應等級
- 取樣室:依取樣對象而異——一般原料取樣不必然需要無塵室等級;無菌原料、高活性 API 或細胞毒性藥物的取樣,需提高潔淨度並可能需要負壓或封閉式取樣設備
- 留樣室、文件區:一般環境
- 試劑儲存:一般環境,但需要溫度控制
如果廠房同時有 GMP 製造的潔淨製程區,QC 微生物區和取樣室的潔淨度規劃要跟製程區的等級對齊——可以對照 無塵室規劃設計與建置工程指南 的潔淨等級分類來確認。
選型建議:規劃化學區和微生物區的隔間時,不要一開始就追求最高潔淨度。先依產品類型、檢測項目、Annex 1 與廠內 SOP做風險評估,把基礎結構(牆、地、空調主機)做扎實,潔淨度等級可以隨產品線升級而調整。一開始就拉到 ISO 5,每年的維護成本會把利潤吃掉。
五、儀器室規劃:HPLC、天平、滴定、UV-Vis、溶離各自的空間需求
化學分析區裡的儀器,每一台都有自己的空間需求。把它們**全部塞進同一間「儀器室」**是最常見的錯誤——HPLC 需要的環境跟分析天平不一樣,跟溶離試驗也不一樣。把這些差異在規劃階段就理清楚,後面儀器到貨時不用一邊用一邊改隔間。
HPLC 室:穩定壓倒一切
HPLC 高效液相層析 是 QC 實驗室最常見也最敏感的儀器之一。它對環境的要求集中在四個面向:
溫濕度穩定。HPLC 對環境條件的要求應以原廠規格、分析方法驗證條件、廠內 SOP 為準。常見的設計起點是溫度 22–24°C、濕度 40–60% RH,溫度波動的常見容忍範圍落在 ±2°C 區間(具體值依儀器型號、檢測器類型、方法靈敏度而異)。對滯留時間、柱溫或檢測器穩定性敏感的方法,應提高溫控精度。短時間溫度波動超過原廠規格範圍,可能讓滯留時間漂移、影響定量準確度。
防震。HPLC 的幫浦、自動進樣器對震動敏感,特別是位於工廠內、靠近重型設備或交通要道的廠房。HPLC 室應遠離壓縮機、離心機、空調主機室;如果無法避免,桌面要採用防震墊或獨立防震桌。
電力穩定。HPLC 系統建議配置 UPS(不斷電系統)或等效的電力保護方案——例如緊急電力、穩壓器搭配資料即時備份、或方法中止 SOP。短時間斷電會讓正在進行的分析中止、可能需要重做樣品;長時間斷電可能讓幫浦、檢測器內的緩衝液乾涸結晶。如果採用 UPS,容量規劃要考量整套系統(幫浦、自動進樣器、檢測器、電腦工作站)的總功率,常見建議是至少能撐 15–30 分鐘讓樣品分析完成或安全關機。具體做法依儀器規格、停電風險、廠內 IT 政策而定。電力配置整體規劃可以參考 機電工程 的服務內容。
廢液處理。HPLC 每天產生的有機廢液(含乙腈、甲醇、緩衝液)量不小。HPLC 室要規劃廢液收集系統,包括防漏托盤、有機 / 水相分流容器、定期清運動線。
分析天平室:對微小擾動極度敏感
分析天平(特別是四位、五位小數天平)對空氣擾動、震動、溫度梯度極度敏感——一陣風吹過、一個人從旁走過,讀數就會跳。
天平室的規劃重點:
- 獨立的 天平桌:實心石材或大理石檯面,重量足夠提供質量阻尼,不跟其他工作檯面共用
- 遠離門口和空調出風口:避免氣流擾動
- 遠離震動源:壓縮機、離心機、人員走動頻繁的區域
- 獨立或局部空調:避免大房間的空調溫度震盪影響讀數
實務上,分析天平不一定需要獨立房間,但至少要有一個獨立角落 + 適當隔屏。五位小數的微量天平則建議獨立小房間,並配置防震桌。
滴定 / 溶離 / KF 水分:通用前處理空間,但要注意排煙與廢液
滴定(含自動電位滴定)、溶離試驗(Dissolution)、KF 水分 這幾類分析常常共用空間,因為它們的工作模式類似——人員手動操作、有部分試劑揮發、有廢液產生。
這個空間的規劃重點是:
- 排煙櫃 處理揮發試劑(甲醇、乙醇、酸類)
- 廢液收集動線(酸鹼分流、有機水相分流)
- 純水供應(DI 或 RO)就近配置
- 桌面材質耐腐蝕(環氧樹脂或酚醛樹脂)
溶離試驗如果是大型製藥廠,通常會獨立成「溶離試驗室」,因為溶離設備本身佔空間(每台至少 6–8 個容器同時運作),且需要恆溫水浴和取樣自動化系統。
UV-Vis、IR:相對單純,但避免日光直射
UV-Vis 分光光度計 和 IR 紅外光譜的環境需求相對單純——溫濕度有控制即可,沒有特別的防震要求。但兩者都要避免日光直射和強光環境,因為光源穩定性可能受外部光線干擾。
實務上 UV-Vis 和 IR 通常放在化學分析區的一個角落,跟 HPLC 共享空調,但桌面位置選在沒有窗戶或加遮光簾的區域。
共用儀器集中 vs 分散的判斷
天平、移液器、純水、烘箱這類「兩邊都會用到」的儀器,到底是集中放一個共用儀器室,還是分散到化學區和微生物區各放一套?
判斷邏輯有兩個:
使用頻率。如果某項儀器在化學區和微生物區的使用頻率都很高,分散配置(各放一台)比較合理;如果只是偶爾用,共用儀器室比較省成本。
交叉污染風險。微生物區和化學區共用一台天平是高風險——化學試劑的微量殘留可能影響微生物樣品。這類儀器強烈建議分開配置。烘箱也類似(化學乾燥和微生物滅菌不應共用)。
純水系統可以共用,但管線要從化學區優先供應、微生物區末端取水,避免微生物迴流污染化學分析。氣體配管也是同樣邏輯,可以參考 氣體管路工程 的整合設計。
一張表看儀器空間需求差異
| 儀器類型 | 溫濕度 | 防震 | 電力 | 排煙 | 純水 | 廢液 |
|---|---|---|---|---|---|---|
| HPLC | 依原廠規格 / 方法(常見 ±2°C / 40–60% RH) | 中 | UPS 建議 / 等效保護 | 不需要 | 必要 | 大量有機 |
| 分析天平 | 防氣流 / 溫度穩定(常見 ±1°C) | 高 | 一般 | 不需要 | 不需要 | 無 |
| 滴定 / KF | 一般 | 低 | 一般 | 局部需要 | 必要 | 中量酸鹼 |
| UV-Vis | 一般 | 低 | 一般 | 不需要 | 必要 | 少量 |
| 紅外光譜 | 中 / 避免高濕 | 低 | 一般 | 不需要 | 不需要 | 無 |
| 溶離試驗 | 恆溫水浴(依藥典 / 方法,常見 ±0.5°C) | 低 | 一般 | 不需要 | 必要 | 中量 |
註:表中的數字皆為常見規劃起點,實際設計值應依儀器原廠規格、方法驗證條件與廠內 SOP 訂定。
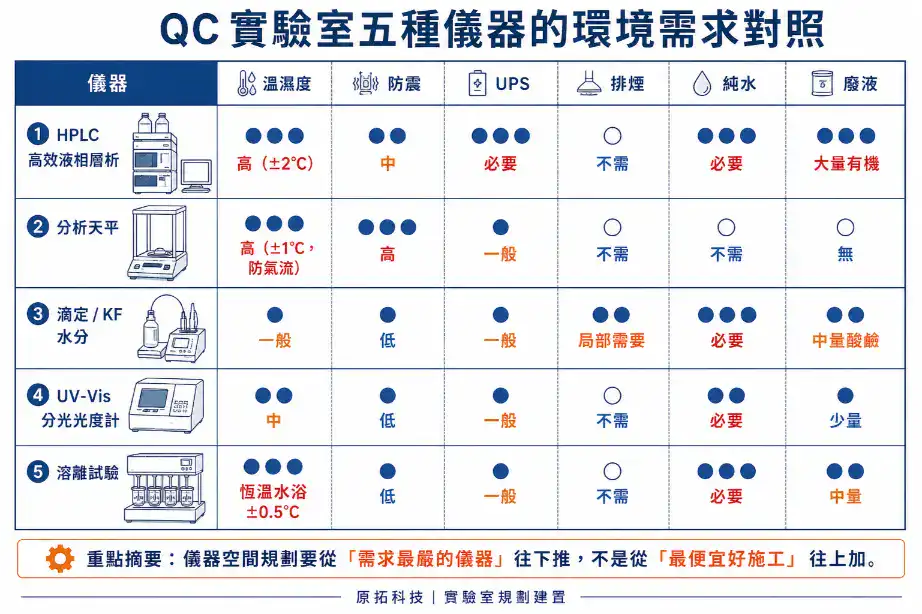
這一節的重點是:儀器空間規劃比較合適的順序是從「需求最嚴的儀器」往下推,而不是從「最便宜好施工」往上加。HPLC 室如果一開始沒把溫濕度、防震、電力保護處理好,後續再加裝時很容易要重拉電、重做隔間。
六、留樣室設計:常被低估的空間
GMP 品管實驗室的留樣室是個有趣的存在——它不執行任何分析,但卻是稽查時必查的空間之一;它不產生任何收入,但每一批產品都要在這裡躺好幾年。很多廠在第一次規劃時把它當成「儲物間」,結果第二年就發現空間不夠、追溯系統亂掉。
留樣的法規依據
PIC/S GMP 第六章對保留樣品(Reference and Retention Samples)有明確規定。基本邏輯是:每一批產品都要保留足夠數量的樣品,用於日後可能的再檢測、品質調查、或主管機關抽驗。
留樣分兩類:
- 參考樣品(Reference Sample):用於日後的再檢測。儲存於可進行檢測的條件下
- 保留樣品(Retention Sample):用於辨識產品(例如完整包裝樣品供日後調查批號、外觀比對)
兩類的儲存條件可能不同,所以留樣室通常不會只有一個區域,而是依儲存條件分成常溫、冷藏、冷凍、避光等不同子區。
留樣期限
PIC/S GMP 規定留樣期限至少保留至產品有效期限後一年。實際期限會因產品類型、市場、客戶端要求而有差異——
- 有效期 2 年的產品,留樣至少保留 3 年(有效期 + 1 年)
- 有效期 3 年的產品,留樣至少保留 4 年
- 部分外銷市場(例如美國 FDA、歐盟 EMA)對留樣的要求可能更嚴
- 原料藥(API)的留樣期限規範略有不同,可參考 ICH Q7
實務上,很多廠會把留樣期限再加 6 個月到 1 年,作為品質調查、客訴處理的緩衝。這個做法不是法規強制,但是業界穩健做法。
留樣量計算與空間規劃
留樣空間規劃最常見的失敗,是用第一年的批次數量規劃。第二年批次數可能翻倍,第三年又再翻倍,原本「剛剛好」的留樣室爆滿。
合理的計算邏輯是:
- 估算 5 年內可能的批次數高峰(不是平均值)
- 每批次的留樣體積(含外包裝、留樣容器、標籤空間)
- 加上樣品移動、清點、銷毀準備的工作空間
- 再額外預留 30–50% 冗餘
這樣計算出的空間,第一年看起來很空,第三年剛好夠用。如果第一年就規劃得剛剛好,第二年就會開始想「要不要把留樣放到普通儲物櫃」——這個念頭出現的當下,留樣管理就已經破口了。
留樣的儲存設備也要分類規劃。常溫留樣可以用一般 藥品安全儲存櫃;冷藏留樣需要實驗室冷藏冰箱(不能用家用冰箱,因為溫度均勻度和監控不符合 GMP 要求),可以參考 實驗室冰箱與冷凍櫃選購比較指南 的選型重點;冷凍留樣需要 -20°C 或更低的實驗室冷凍櫃;高活性 API 或敏感藥物可能需要 -80°C 超低溫冷凍櫃。
文件追溯
留樣的工作除了「把樣品放著」,每個留樣都要有完整的文件追溯——
- 批次號、製造日期、效期
- 入庫日期、儲存位置(編號到櫃號、層號)
- 入庫時的環境條件、入庫人員簽核
- 定期檢查紀錄(外觀、容器完整性、儲存環境)
- 銷毀日期、銷毀方式、銷毀見證人
這些紀錄通常進入 LIMS 或專門的留樣管理系統。設計留樣室時,入口要有電腦工作站讓樣品管理員即時記錄,不能事後補;櫃位編號要清楚到每一格,不能用「大概那一區」帶過。
常見踩坑:留樣室的環境監控(溫度、濕度、警報)跟其他空間共用,是稽查重點觀察項目。常溫留樣室如果是冷氣壞掉沒人發現,溫度爆衝到 30°C 以上又超過幾小時,所有留樣的「儲存條件符合性」就要重新評估。獨立的環境監控 + 24 小時警報 + 假日值班 SOP,這三件事少一件都會被稽查抓。
七、資料完整性與文件管理空間
寫到資料完整性,很多人第一反應是「這是 IT 的事,跟空間規劃有什麼關係?」關係很大。資料完整性的稽查重點,有一半以上會落在「物理空間有沒有支持資料的可追溯、可歸屬、即時記錄」。
為什麼資料完整性需要物理空間支持
回到 ALCOA+ 的九個原則。其中至少四個原則跟空間配置直接相關:
- Attributable(可歸屬):每筆資料都能查到是誰做的。空間上要做到——每個工作站只給特定人員使用,或有獨立帳號登入;不能多人共用一台 LIMS 終端機而沒有切換帳號的習慣
- Contemporaneous(即時記錄):資料要在工作完成的當下寫,不是事後補。空間上要做到——每台儀器旁邊都要有書寫或電子記錄空間,分析人員不能離開儀器去找紀錄本
- Original(原始資料):原始紀錄要保存原貌。空間上要做到——紙本紀錄有受控的儲存空間,不能跟一般文件混放;電子原始資料的伺服器有獨立的機房或受控空間
- Enduring(持久保存):資料要保存完整的法規期限。空間上要做到——文件儲存空間能滿足留檔期限(通常是產品效期+1 年到+5 年不等),不能因為換系統、搬廠就遺失
物理動線上的「紙本與電子簽核空間」
很多 GMP QC 實驗室同時使用紙本和電子記錄。完全電子化的廠房比較少,因為:
- 部分舊系統還在使用紙本(遷移成本高)
- 部分稽查員仍習慣看紙本紀錄
- 資料完整性要求電子系統符合 21 CFR Part 11 / EU Annex 11,全面電子化要花時間
紙本與電子並存的環境,空間上要規劃兩套並行的工作流:
- 每台儀器旁有「紙本紀錄空間」(書寫桌面 + 紀錄本儲存)
- 每台儀器旁有「電子紀錄空間」(LIMS 終端 + 電子簽核站)
- 文件區有「紙本歸檔櫃」(受控、有編號、有借閱紀錄)
- 文件區有「電子備份儲存」(獨立伺服器或受控的雲端空間)
這代表化學分析區的桌面深度通常要比一般化學實驗室多 20–30 公分,因為要放紀錄本和電腦終端機。一開始沒規劃,後來再加桌子,會擠壓到儀器操作空間。
文件區獨立、不與儀器區混用
QC 實驗室的「文件區」是個獨立功能空間,不應該散落在儀器區。文件區的功能包括:
- SOP、批次紀錄的審核(QA 主管的工作站)
- 報告撰寫(分析人員審完原始紀錄後撰寫 CoA)
- 統計分析(趨勢圖、控制圖、年度品質檢討)
- 受控文件的存取(紙本歸檔、電子文件下載)
文件區獨立的好處是——人員不會在儀器運作時被打擾,分析的專注度提升;同時,文件區的權限管理可以更嚴格(誰能進、誰能借、誰能改)。
稽查員看到的「物理線索」
PIC/S 稽查員在現場看資料完整性時,會注意這些物理細節:
- 紀錄本的字跡是否一致(多人寫一本?事後補寫?)
- 簽名筆跡是否真實(影印的簽名?代簽?)
- 時間戳記是否合理(凌晨三點的紀錄?同一人在兩個地點同時簽名?)
- 紀錄本的保管位置(不在受控空間?普通抽屜?)
- 廢棄紀錄的處理(直接丟垃圾桶?沒有銷毀紀錄?)
- LIMS 的權限設定(共用帳號?沒有變更追蹤?)
這些細節背後的物理規劃就是——紀錄要有自己的「家」:書寫位置、儲存位置、審核位置、銷毀位置都要明確。如果一份紀錄的「家」不確定,稽查員會懷疑整套資料完整性的執行強度。
八、QC 實驗室的儀器與空間驗證:IQ/OQ/PQ
GMP QC 實驗室的儀器和空間,安裝完成後通常還要經過 IQ/OQ/PQ 三階段驗證,才能正式投入 GMP 環境使用。這套驗證制度是 GMP 的主要特徵之一,也是稽查時必查的項目。
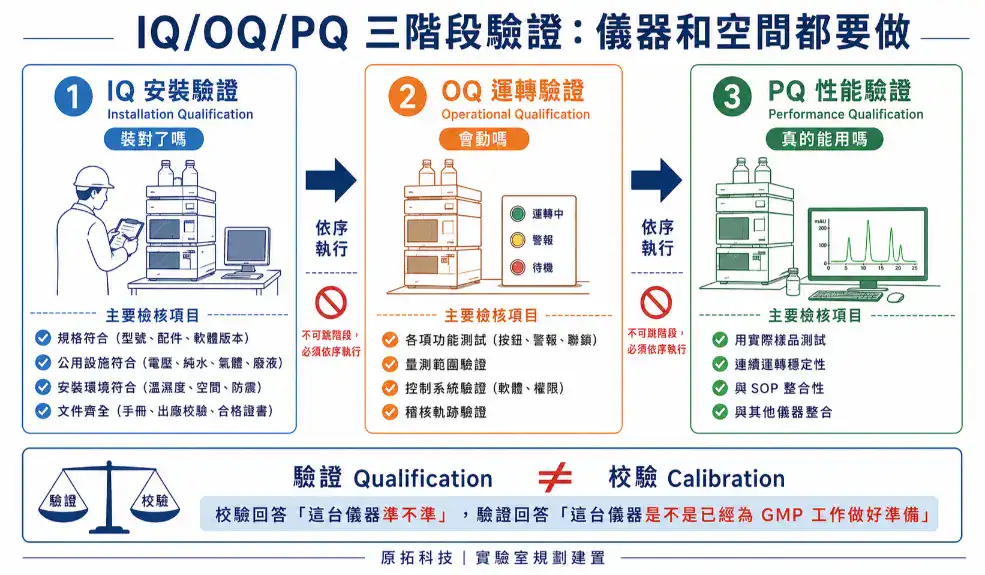
三階段驗證的意義
IQ(Installation Qualification,安裝驗證):確認儀器或設備依照規格正確安裝。包括:
- 規格符合性(型號、配件、軟體版本)
- 公用設施符合(電壓、電流、氣體、純水、廢液)
- 安裝環境符合(溫濕度、空間、防震)
- 文件齊全(操作手冊、出廠校驗報告、合格證書)
OQ(Operational Qualification,運轉驗證):確認儀器或設備在規定的運轉範圍內,功能正常。包括:
- 各項功能測試(按鈕、警報、聯鎖)
- 量測範圍驗證(在 spec 範圍內讀數正確)
- 控制系統驗證(軟體、權限、稽核軌跡)
PQ(Performance Qualification,性能驗證):確認儀器或設備在實際使用條件下,能持續產生符合預期的結果。包括:
- 用實際樣品測試(不是標準品)
- 連續運轉穩定性
- 與其他儀器、SOP 的整合性
三階段是依序執行的邏輯——通常 IQ 完成後才進入 OQ、OQ 完成後才進入 PQ。如果某階段有部分項目不合格,依各廠 SOP 與偏差管理流程處理(補正、變更、書面決定後續)。每階段的紀錄都要進入 GMP 文件系統。具體執行範圍與判定標準依各廠 SOP、儀器類型、產品風險而異。
空間驗證項目
不只儀器要驗證,整個 QC 實驗室的空間本身也要驗證。空間驗證項目包括:
- 潔淨度(依分區的等級要求進行粒子計數)
- 溫濕度均勻性(在不同位置量測,確認不超過 SOP 規定範圍)
- 壓差梯度(化學區、微生物區、走道之間的壓差)
- 氣流模式(用煙霧測試確認氣流方向)
- 照度(確認工作面照度足夠進行精細工作)
- 噪音(高噪音可能影響分析人員的專注)
這些驗證通常委託第三方公司執行,因為需要校驗過的儀器和有資格的人員。每一份驗證報告都要進入文件系統,作為日後再驗證的基準。
驗證 vs 校驗的差別
驗證(Qualification)跟校驗(Calibration)是兩件事,不能混為一談。
- 校驗:確認儀器的讀數準確。例如天平用標準砝碼校驗,確認 100g 砝碼讀出來是 100.00g
- 驗證:確認儀器在 GMP 系統下適合使用。校驗只是驗證的一部分
簡單說,校驗回答「這台儀器準不準」,驗證回答「這台儀器是不是已經為 GMP 工作做好準備」。GMP 環境下兩者都需要,且都要有獨立紀錄。
重新驗證的時機
驗證不是一次做完就一勞永逸。重新驗證的時機包括:
- 定期再驗證:常見頻率為每年一次(PQ)或每 2–3 年一次(OQ),實際週期依儀器類型、使用強度與廠內 SOP 而定
- 變更後:儀器搬遷、軟體升級、規格修改、零件更換後,要做相關項目的再驗證
- 環境變更:實驗室隔間改動、空調系統升級、新增儀器影響到既有空間,要做空間再驗證
- 稽查缺失改善後:稽查發現的問題改善後,要做相關再驗證
管理建議:把驗證當成「會持續發生的工作」來規劃,不是「裝好就結束」的一次性任務。每年的 QC 實驗室預算裡,要包含驗證費用、第三方服務費、以及再驗證期間的儀器停機成本。
九、稽查友善設計:實驗室在外觀上就讓稽查員放心
PIC/S 稽查員走進 QC 實驗室的第一個小時,看的不是文件,是物理空間有沒有「在管理的樣子」。空間設計如果一眼就讓人感覺亂、混淆、流向不清,後續再用 SOP 解釋通常事倍功半。
「稽查友善設計」不是賄賂稽查員的概念,是透過物理線索讓稽查過程順利的設計思維。
稽查員會看的物理線索
從業界經驗整理,稽查員在現場通常會注意這些細節:
- 動線標示:走廊、入口有沒有清楚標示分區?人流、物流、樣品流的方向有沒有圖示?
- 設備認證貼紙:每台儀器旁有沒有 IQ/OQ/PQ 的認證貼紙?貼紙日期是不是最新的?
- 校驗狀態標示:儀器有沒有「校驗中」、「使用中」、「待校驗」的狀態標籤?
- 留樣標籤:留樣容器標籤是否清楚、字跡是否工整、有沒有破損或字跡模糊?
- 清潔狀態:地板、桌面、儀器外觀的清潔程度?清潔紀錄有沒有掛在現場?
- 廢棄物分類:化學廢液、生物廢棄物、一般垃圾的分類桶是否清楚?
- 緊急應變設備:緊急沖淋洗眼器、滅火器位置是否合規、是否有定期檢查紀錄?
這些細節單獨看都不大,加總起來就是稽查員對「整個實驗室管理水準」的第一印象。
容易被抓的設計缺陷
從稽查實務看,最常被抓的設計缺陷有幾個:
取樣與檢測共用空間。沒有獨立取樣室,取樣就在化學分析區角落進行。稽查員一看就會問:「樣品的接收動線在哪裡?怎麼確保新樣品和已分析樣品不混淆?」若空間本身無法支持樣品狀態分離,後續通常只能透過隔間調整、權限管制或流程重設來補強。
留樣室紊亂。留樣容器沒有清楚編號、儲位沒有圖示、進出沒有紀錄。稽查員會直接抽查某批次的留樣,如果找不到、或標籤模糊、或環境條件不符,整套留樣管理就會被列為缺失。
文件混在儀器旁。SOP、紀錄本、原始數據紙條全部堆在 HPLC 旁邊。稽查員會想:「這些文件的版本控制在哪?有沒有過期版本還在使用?」
廢棄物分類不清。化學廢液和一般垃圾混在一起,或廢液桶沒有標示成分。這個問題不只是稽查缺失,更是職安和環保問題。
三個「外觀就看得出在管理」的設計細節
要讓實驗室在外觀就傳達「在管理」的訊息,三個常見有效的設計細節:
依顏色分區的牆面或地板標示。化學區用一種顏色(例如藍色),微生物區另一種(例如綠色),走道、共用區再一種(例如灰白)。顏色一致性讓稽查員一眼看出空間邏輯。無縫地板 的設計可以從顏色分區下手。
清楚的人流物流方向標示。地板上用箭頭、牆面上用圖示,標出「樣品從這邊走、人員從那邊走、廢棄物往這邊去」。即使沒有 SOP 解釋,看圖就懂。
設備認證貼紙統一規格。所有儀器的 IQ/OQ/PQ、校驗、最後維護日期,用同一種規格的貼紙、貼在同一個位置(例如儀器右上角)。稽查員掃一眼就能看到所有狀態標示。
管理建議:「稽查友善」與其說是表面功夫,不如說是把日常管理的成果用物理線索表達出來。如果日常管理本身做得好,這些設計能讓稽查員更快看到事實;如果日常管理本身有缺陷,光靠表面設計能補的部分有限。把焦點放在日常管理,再用設計讓它「容易被看見」。
十、QC 實驗室規劃流程:從需求訪談到驗收啟用
把前面九章整合成一條時間軸,QC 實驗室的規劃流程可以拆成七個步驟。這個流程跟主文 實驗室規劃設計完整手冊 的七步驟有對應關係,但每一步都加入 GMP 特殊要求。
步驟一:需求訪談
不只問「要做什麼分析」,還要問:
- 產品線(西藥 / 保健食品 / 化妝品 / API)和劑型
- 預期批次數(第一年 / 第三年 / 第五年)
- 主要客戶端要求(外銷市場、客戶稽查標準)
- 既有實驗室狀況(新建 / 改建)
- 預算分配(建置 / 設備 / 驗證 / 運轉成本)
GMP 環境下,未來擴充規劃比一般實驗室更重要——因為改建涉及驗證、空間動線可能要重新規劃,成本是新建時的數倍。
步驟二:法規盤點
依照產品線和市場,盤點適用的法規:
- 西藥:PIC/S GMP(衛福部公告版本)+ TFDA 補充指引
- 保健食品:食品工廠 GMP + 食藥署指引
- 化妝品:化粧品優良製造準則
- 外銷市場:FDA 21 CFR Part 211(美國)、EU GMP(歐盟)、PMDA(日本)等
- 適用劑型的特殊規範(無菌製劑、高活性 API、生物製劑)
法規盤點的結果會直接影響分區、潔淨度、文件系統的設計。如果法規層面跨多個市場,要以最嚴的標準為設計基準,而不是平均值。
步驟三:動線與分區設計
依照樣品單向管理邏輯和八大功能區,畫出第一版平面圖。重點檢查:
- 樣品從取樣到留樣是否單向管理、狀態清楚
- 化學區和微生物區的分隔設計(依風險評估決定 HVAC 工程層級)
- 取樣室是否獨立
- 留樣室空間是否預留 30–50% 冗餘
- 人員、物流、廢棄物動線是否分離
這一步通常需要跟使用部門(QC、QA)和工程部門共同討論,多次修改後才能定稿。
步驟四:儀器規劃與環境需求
依照分析項目和未來擴充,列出儀器清單。每台儀器確認:
- 環境需求(溫濕度、防震、UPS、純水、氣體)
- 公用設施需求(電力、排水、廢液收集)
- 安裝空間(含搬運路徑、維修空間)
- IQ/OQ/PQ 的執行單位(原廠 / 第三方)
儀器規劃完成後,可能要回頭調整步驟三的平面圖。
步驟五:文件系統整合
QC 實驗室不是獨立運作的——它要跟生產(批次紀錄)、QA(批次放行)、倉儲(取樣、入庫)、ERP(成本、庫存)整合。文件系統規劃包括:
- LIMS(實驗室資訊管理系統)的選型與導入
- ERP / MES 的介接
- 紙本與電子並行的工作流設計
- 21 CFR Part 11 / EU Annex 11 符合性
文件系統的導入時程通常比實體建置長,建議從專案開始就同步規劃,不要等實驗室蓋好才開始。
步驟六:驗證與確效
實體建置完成後,進入驗證階段。驗證項目包括:
- 空間驗證(潔淨度、溫濕度、壓差、氣流)
- 公用設施驗證(純水、空調、氣體、UPS)
- 儀器 IQ/OQ/PQ
- LIMS / 電子系統驗證(CSV,Computer System Validation)
驗證階段通常 2–4 個月,依規模而異。第三方驗證公司的排程要提前 1–2 個月確認,否則會耽誤啟用時程。
步驟七:試運轉與稽查準備
驗證完成後不等於可以正式運作。試運轉階段(通常 1–2 個月)的工作包括:
- 用實際樣品跑完整批次的 QC 流程
- 訓練操作人員(特別是 GMP、SOP、LIMS 操作)
- 模擬稽查(內部稽核 + 外部顧問模擬 PIC/S 稽查)
- 完成試運轉缺失改善
稽查準備的重點是「讓物理空間說出符合 SOP 的故事」——稽查員走進來的第一個小時,能不能用空間上的物理線索講清楚分區、動線、文件、驗證?這個準備如果做好,第一次正式稽查通常會順利。
完整的規劃服務可以參考 實驗室規劃設計與建置服務 的服務內容。
GMP 品管實驗室 FAQ
Q1:GMP 品管實驗室和 ISO 17025 認證實驗室有什麼差別?
兩者的邏輯側重不同。GMP 品管實驗室是製造端的內部品管,目的是確保自家產品的批次合格、可追溯;ISO 17025 是通用實驗室能力標準,可以用於第三方檢驗實驗室或內部品管。
實務上,GMP QC 實驗室可以同時取得 ISO 17025 認證(特別是有對外接案的情況),但反過來不一定——一個 ISO 17025 實驗室不會自動符合 GMP 規範。GMP 對「批次追溯、留樣、稽查路徑」的要求比 ISO 17025 更具體;ISO 17025 對「方法驗證、量測不確定度、儀器校驗」的要求則比 GMP 更技術導向。
如果你的廠房同時要符合兩者,規劃時以 GMP 為基底,再把 ISO 17025 的方法驗證、不確定度評估等技術要求疊加上去。
Q2:PIC/S GMP 對 QC 實驗室空間有什麼具體規定?
最直接相關的是 PIC/S GMP 第三章「廠房設施與設備」和第六章「品質管制」。第三章規定儀器分析、生物試驗、微生物試驗應彼此分隔——這是空間分區的法規依據。第六章規定保留樣品的種類、數量、儲存條件、保留期間——這是留樣室規劃的法規依據。
但 PIC/S GMP 是原則性規範,不會寫到「化學區要幾平方米」「天平室要幾度」這種細節。具體尺寸、溫濕度範圍要依產品類型、儀器規格、廠內 SOP 自行訂定,並透過驗證來證明合理性。
Q3:化學分析區和微生物分析區一定要實體分開嗎?
實體分隔是 PIC/S GMP 第三章的法規要求——但「分隔」指的是物理區隔,沒有規定一律要採用完全獨立的 HVAC 系統。具體工程做法(共用空調 + 獨立排氣、部分區域獨立 HVAC、完全獨立 HVAC)應依風險評估決定,考量產品特性、操作型態、微生物項目(是否涉及無菌試驗)和空間規模。
對於有揮發性溶劑、粉塵、高活性物質、無菌試驗或高污染風險的場景,應優先採用獨立或明確分區控制的 HVAC 設計,避免空氣交互污染。對於風險較低的一般 QC 環境,實體隔間搭配獨立排氣與緩衝區可能就足夠。設計階段先做風險評估,把工程設計層級訂清楚,才不會過度設計或設計不足。
Q4:留樣室空間要多大?怎麼計算?
合理的計算邏輯是:估算 5 年內的批次數高峰(不是平均值)× 每批留樣體積(含外包裝、容器、標籤)× 留樣期限 × 1.3–1.5 倍冗餘。這是規劃初估的常見起點,實際空間需求需依個案確認。
PIC/S GMP 對保留樣品的最低保留期間規定是「產品有效期 + 1 年」,原料藥(API)的留樣期限規範略有不同,可參考 ICH Q7。實務上很多廠會再加 6 個月到 1 年作為 OOS/OOT 調查、客訴處理、客戶端要求的緩衝。
最常見的失敗是用第一年的批次數規劃,第二年就爆滿。一次到位的留樣室會比分階段擴充省成本——但實際金額仍須依個案專案條件評估。
Q5:資料完整性對空間規劃有什麼影響?
ALCOA+ 原則中,至少有四個跟空間直接相關:每個工作站要能識別個人身分(Attributable)、每台儀器旁要有即時記錄空間(Contemporaneous)、原始紀錄要有受控儲存空間(Original)、文件儲存空間要滿足完整法規期限(Enduring)。
實務上,這代表:化學分析區的桌面要比一般化學實驗室深 20–30 cm(放紀錄本和電腦終端);文件區要獨立、不跟儀器混用;紙本歸檔櫃要受控、有借閱紀錄;電子備份伺服器要有獨立的空間或受控環境。
Q6:製藥廠新建 GMP QC 實驗室的時程大概多久?
依規模、廠內既有條件、法規範圍而異。從需求訪談到正式啟用,常見的規劃起點是:
- 小型廠(500–1,000 m²):12–18 個月
- 中型廠(1,000–2,000 m²):18–24 個月
- 大型廠(2,000 m² 以上):24–36 個月
實際時程仍須依個案條件確認。時程包括需求訪談、法規盤點、設計、施工、驗證、試運轉、稽查準備。其中驗證階段常占整個專案 20–30% 的時間,是很多人低估的部分。
如果是改建(既有廠房),時程不一定比新建短——因為改建涉及不停產、舊設備搬遷、暫時性 SOP 變更等複雜性。
Q7:怎麼選 GMP 品管實驗室規劃廠商?
GMP QC 實驗室是跨領域整合題——不只是空間規劃,還涉及 PIC/S 法規、儀器選型、文件系統、驗證流程。選廠商時建議看幾個面向:
- 是否有 GMP 廠房規劃實績:不只是「實驗室規劃」實績,要有 GMP 環境的實績
- 是否能跨部門協調:規劃、機電、儀器、驗證通常不是同一家做,但要有人能整合多方廠商
- 是否熟悉台灣 TFDA 稽查重點:法規條文是國際的,但稽查重點和實務做法是台灣在地的
- 是否能提供完整的後續服務:驗證、再驗證、稽查模擬、缺失改善都是長期需求
規劃廠商的選擇對 GMP 廠來說是長期合作關係,不只是一次性的建置。
Q8:保健食品工廠或化妝品 GMP 廠是不是也適用同一套規劃?
硬體規劃邏輯八成相通,差異主要在法規層面。三產業差異對照如下:
| 比較項目 | 西藥廠 PIC/S GMP | 保健食品 GMP | 化妝品 GMP |
|---|---|---|---|
| 主管機關 | 衛福部食藥署 | 衛福部食藥署 | 衛福部食藥署 |
| 法規依據 | PIC/S GMP(強制) | 食品安全衛生管理法 + 食品工廠 GMP / HACCP | 化粧品優良製造準則(強制) |
| 留樣期限 | 產品效期 + 1 年(最低) | 依產品而異,通常 1–3 年 | 產品效期 + 1 年(最低) |
| 微生物特殊項目 | 無菌試驗、內毒素、菌數限度 | 致病菌、總生菌數、衛生指標菌 | 防腐效能測試(PET)、微生物挑戰測試 |
| 化學特殊項目 | 含量、雜質、溶離、安定性 | 營養標示、農藥殘留、重金屬 | 重金屬、防腐劑、塑化劑 |
| 文件 / 資料完整性要求 | ALCOA+(PIC/S PI 041-1) | 一般 GMP 紀錄要求 | 一般 GMP 紀錄要求 + 部分品項 ALCOA+ |
動線、分區、儀器配置可以直接套用本文;法規層面建議搭配各產業專業顧問或法規事務人員確認。
需要 GMP 品管實驗室規劃協助?
GMP 品管實驗室不是一般實驗室加上 SOP——它從動線、分區、儀器、文件、驗證每一步都依 PIC/S 法規邏輯設計。原拓科技協助西藥廠、保健食品廠、化妝品 GMP 廠的 QC 品管實驗室規劃、建置、驗證準備,從需求訪談到稽查準備提供完整服務,可以參考 實驗室規劃設計與建置服務。
如果你正在規劃新建 QC 實驗室,或既有實驗室面臨 PIC/S 稽查改善需求,可以先 聯繫我們 討論現場條件與改善方向。
相關產品分類
相關服務
- 實驗室規劃與建置經理人 — 規劃、機電工程、空間裝修、設備整合一站式服務
- 實驗室建置完整解決方案 — 規劃 + 工程 + 設備統包
- 科學儀器經理人 — 跨品牌實驗室儀器選型與配置顧問
