
一間生技研發實驗室的規劃失誤,通常不是單純少買一台生物安全櫃或培養箱——設備清單相對容易列出來,真正困難的是把設備和空間整合起來。空間蓋好之後才發現:操作人源細胞株的區域和一般微生物培養共用同一套空調迴路,廢棄物從培養區搬到高壓滅菌室要穿過半條走廊,或者 BSC 排氣接上去之後才知道既有風管的靜壓根本不夠。
這些問題有一個共通點——它們都不是設備的問題,而是空間規劃階段沒有把「生物安全分級」當成設計的起點。生技醫藥研發實驗室和一般化學實驗室、品管實驗室的規劃邏輯有很不一樣的起點,而這個差異從第一張平面圖開始就會影響後續每一個決定。
這篇指南是寫給正在規劃或改建生技研發實驗室的你——不管是新創生技公司的第一間實驗室,還是既有研究機構要擴建細胞培養或基因工程的空間。我們會從生技 R&D 實驗室的規劃邏輯講起,一路走過 BSL 分級對應、功能分區、動線設計、環境控制、設備配置和法規框架,把規劃階段容易踩的坑提前攤開來看。
適用範圍說明:本文聚焦於生技醫藥研發端的實驗室規劃,例如細胞培養、微生物操作、分子生物、基因工程與早期研發場景。若涉及臨床用細胞製備、GTP、GMP 製造、BSL-3 或特殊病原體操作,空間條件、潔淨等級、壓差、驗證與主管機關要求會明顯提高,需另依專案風險與法規要求規劃。本文中的分區、壓差與設備配置屬於規劃起點與概念性框架,不應視為固定規格,實際設計應由使用單位、生安/IBC、環安衛、HVAC 與設備廠商共同確認。製造端品管實驗室(PIC/S GMP QC)的規劃邏輯不同,請參閱 GMP 工廠 QC 品管實驗室規劃指南。
一、生技醫藥研發實驗室與一般實驗室的四個差異
生技研發實驗室和化學分析實驗室、品管實驗室長得可能很像——都有實驗桌、排煙櫃、培養箱、冰箱。但規劃邏輯不同,設計出來的空間會往完全不同的方向走。這裡把三類實驗室最常被混淆的差異整理出來,方便你在規劃初期就把方向定對。
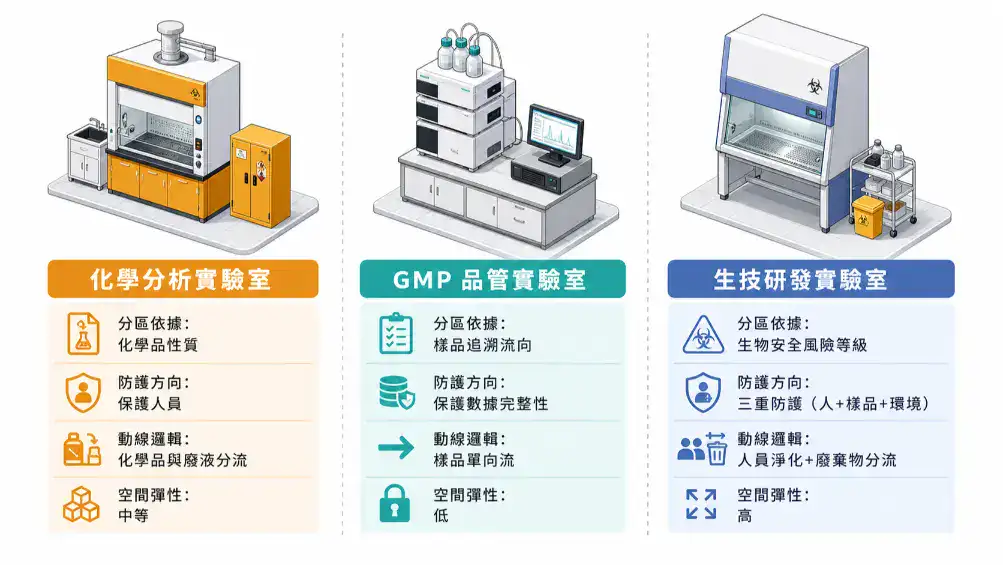
| 比較維度 | 化學分析實驗室 | GMP 品管實驗室 | 生技研發實驗室 |
|---|---|---|---|
| 分區依據 | 化學品性質(酸鹼、有機、高溫) | 樣品追溯流向(取樣→檢測→報告→留樣) | 生物安全風險等級(BSL-1 / BSL-2) |
| 法規主軸 | 毒化物管理、職安法 | PIC/S GMP、TFDA、ICH | 感染性生物材料管理辦法、基因重組實驗守則 |
| 操作對象特性 | 化學品(無活性,風險來自毒性/腐蝕性/可燃性) | 成品/原料/中間體(有明確批次編號,追溯是重點) | 活的生物體(細胞、微生物、病毒載體——操作對象本身就是風險源) |
| 防護方向 | 保護人員不接觸化學品 | 保護數據完整性 + 避免交叉污染 | 三重防護:保護人、保護樣品、保護環境 |
| 動線邏輯 | 化學品和廢液分流 | 樣品單向流(不可逆向) | 人員淨化 + 廢棄物分流(污染防護梯度) |
| 空間彈性需求 | 中等(排煙櫃位置相對固定) | 低(法規框架限制變更彈性) | 高(R&D 專案更替快,空間要能適應不同操作需求) |
看完這張表,你會發現一個特別的地方:生技研發實驗室的防護方向是「三重」的。化學實驗室主要保護人不接觸有害物質;品管實驗室主要保護數據和樣品的完整性。但生技 R&D 實驗室要同時處理三個方向——操作人員不能被生物材料感染(人員防護),培養中的細胞不能被外界微生物污染(產品/樣品防護),實驗室內的生物材料不能洩漏到外部環境(環境防護)。
這三個防護方向會直接影響設備選型(BSC 的類型)、空調設計(正壓還是負壓)、動線規劃(人和廢棄物怎麼走),以及幾乎所有後續的設計決策。
常見踩坑:有些公司在規劃初期把生技研發實驗室當成「有培養箱的化學實驗室」來設計,等到 IBC(生物安全委員會)實地查核時才發現空調壓差不對、BSC 排氣沒有預留、廢棄物動線不符合規定,改起來的成本和時間往往遠超過當初多花一點心思做對的代價。
二、BSL 生物安全分級與實驗室硬體對應
在生技研發實驗室的規劃中,BSL(Biosafety Level,生物安全等級)分級是所有設計決策的起點。你操作的生物材料屬於哪個風險等級,會連動決定 BSC 要不要裝、空調壓差怎麼設計、門禁要不要做、廢棄物怎麼處理。
BSL 的規劃應參考疾管署「實驗室生物安全技術規範及指引」專區的相關文件、感染性生物材料管理辦法、機構 IBC/生安會要求,以及實際的風險評估結果。對多數生技研發公司而言,最常碰到的是 BSL-1 和 BSL-2,少數涉及高風險病原體的研究才會需要 BSL-3。
BSL-1 和 BSL-2 的硬體差距,比你想的大
BSL-1 的硬體需求相對單純,通常可在一般實驗桌與基本通風條件下進行低風險操作,不要求特殊壓差或高等級門禁。但仍需基本的實驗室管理、進出管制、清潔消毒與人員訓練——BSL-1 不等同於一般辦公或教學空間。適用於已確認對健康成人不致病的微生物操作,例如非病原性大腸桿菌、枯草桿菌等教學或基礎研究用菌株。
但只要你的研究涉及人源細胞株、RG2(Risk Group 2)等級的病原體、特定基因重組微生物、病毒載體,或其他可能對人員或環境造成中度風險的生物材料,通常就需要採 BSL-2 操作原則。實際等級仍應依材料來源、操作方式、氣膠風險與 IBC/生安單位審查確認。這一跳,硬體需求會有明顯的升級:
- 生物安全櫃(BSC):可能產生氣膠、飛濺或涉及 RG2/人源材料的操作,應使用 Class II BSC 或其他合適的初級阻隔設備
- 高壓滅菌鍋:BSL-2 實驗室內或就近可及處應配置高壓滅菌鍋。受感染性材料污染或具生物風險的廢棄物,離開實驗區前應依 SOP 滅活或以合規方式處理
- 定向氣流:實驗區域的氣流方向應從低風險區流向高風險區(走廊 → 實驗室內部)
- 門禁管制:BSL-2 區域應有門禁或管制措施,限制非授權人員進入
- 洗手設施與緊急沖淋:實驗室內應設置洗手槽(建議免手動式),走廊可及處應有緊急沖淋洗眼器
- 生物安全標誌:入口處張貼生物危害標誌,載明 BSL 等級、負責人、緊急聯絡資訊
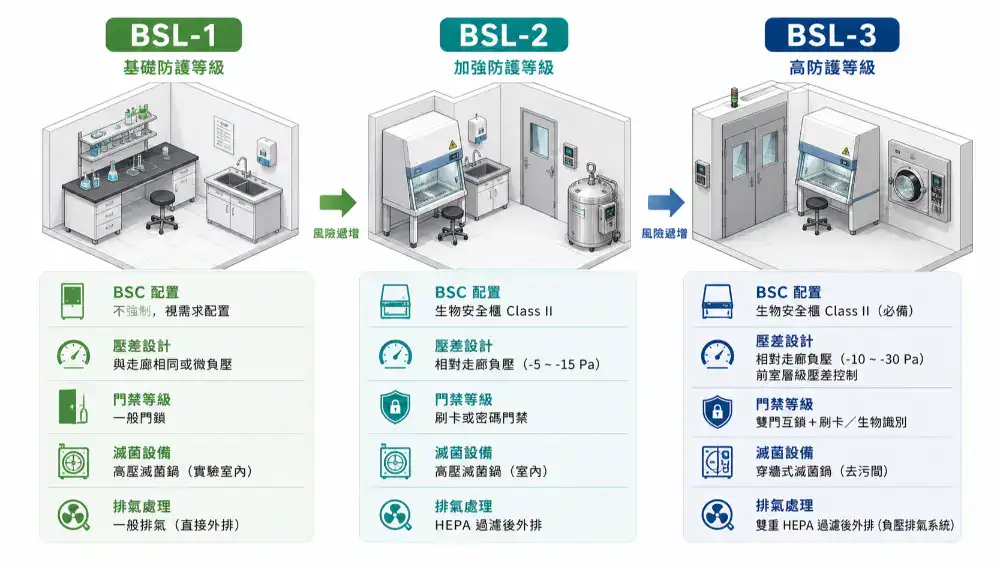
下面這張表把 BSL-1 到 BSL-3 的硬體需求攤開比較,方便你在規劃初期快速對照:
| 硬體項目 | BSL-1 | BSL-2 | BSL-3 |
|---|---|---|---|
| 生物安全櫃 | 通常不要求;依操作風險配置 | 可能產生氣膠、飛濺或涉及 RG2/人源材料等風險操作時,使用 Class II BSC 或合適初級阻隔設備 | 依病原體、操作風險與設施設計選擇 Class II 或 Class III BSC |
| 空調壓差 | 通常不要求特殊壓差 | 依風險評估設計定向氣流;高風險操作區可規劃相對負壓 | 負壓梯度,排氣經 HEPA 過濾,需現場驗證 |
| 門禁 | 基本進出管理 | 管制非授權人員進入 | 受控入口、前室/緩衝區;是否採雙門互鎖依規範與設施設計確認 |
| 高壓滅菌鍋 | 依操作需求配置 | 實驗室內或就近可及處配置 | 通常需在阻隔區內或透過穿牆式設備處理 |
| 洗手設施 | 應有 | 應有(建議免手動式) | 出口附近設置免手動式洗手設施 |
| 窗戶 | 依一般實驗室管理 | 建議不可開啟或受控 | 密封 |
| 排氣處理 | 一般通風 | 依操作與風險評估,避免污染空氣回流至低風險區 | 排氣經 HEPA 過濾,壓差依 BSL-3 設計驗證 |
| 廢棄物處理 | 依一般實驗室分類 | 具生物風險廢棄物依 SOP 滅活、滅菌或合規清運 | 通常需在阻隔區內完成滅活或依規範處理 |
| 人員防護 | 實驗衣、手套等基本 PPE | 實驗衣、手套、護目或面部防護,依操作風險配置 | 依病原體與操作風險配置防護衣、呼吸防護等 |
BSL-2 不等於整間實驗室都要負壓
這是一個常見的誤解,也是規劃階段常被過度設計的地方。BSL-2 的要求是「定向氣流」——空氣從乾淨區流向污染風險較高的區域——而不是「整間實驗室都要維持全負壓環境」。
實務上,BSL-2 實驗室的壓差設計會依區域的風險等級做分層。涉及感染性材料操作或氣膠產生風險較高的區域(例如細胞培養室操作人源細胞株),可評估相對負壓或加強局部排氣。但試劑配製區、儀器分析區這些不直接操作感染性材料的空間,不一定需要套用相同壓差。
壓差設計依區域風險評估決定,不是一刀切。過度設計不只增加空調成本,也會讓日常維護變得更複雜。
GTP 與特殊研發場景
如果你的研發方向涉及細胞治療產品(例如 CAR-T、間質幹細胞),那空間規劃就不只是 BSL 的問題,還會涉及 GTP(人體細胞組織優良操作規範)的要求。GTP 或細胞治療製備空間的關鍵操作通常需在 ISO Class 5 等級的主要操作區或等效設備中進行,並搭配相對應的背景環境、人員更衣、物料傳遞、壓差與環境監測設計。實際潔淨等級與配置應依製程特性、GTP 要求與主管機關審查結果確認,不能直接套用一般 BSL-2 R&D 的標準。
GTP 的規劃邏輯介於「R&D 實驗室」和「GMP 製造廠」之間——有潔淨等級要求,但不像 GMP 那樣有完整的批次放行和品管架構。如果你的研發路徑預計會走到臨床試驗甚至商業化,在規劃初期就把 GTP 的空間需求考慮進去,會比後來改建省事得多。
對了,BSL-3 的建置在一般生技研發公司中相對少見,多集中於大型研究機構、醫學中心或國家級研究單位。如果你的研究確實涉及 RG3 等級的病原體,BSL-3 的設計要求(負壓梯度、受控入口與前室、排氣 HEPA 過濾、穿牆式滅菌鍋等)遠比 BSL-2 複雜,建議從規劃初期就由具 BSL-3 實績的生物安全、HVAC 與驗證團隊共同介入。
三、生技研發實驗室的功能分區設計
功能分區是生技研發實驗室規劃的骨架。分區做得好,後面的動線、空調、設備配置都會順著走;分區沒想清楚,後面每一步都在補救。
生技 R&D 實驗室的分區邏輯,和化學實驗室不太一樣。化學實驗室通常以「化學品性質」分區(酸區、鹼區、有機溶劑區);品管實驗室以「樣品流向」分區(收樣→前處理→檢測→報告→留樣)。生技研發實驗室的分區邏輯是潔污梯度——從最乾淨的區域(細胞培養室)到最髒的區域(廢棄物處理/滅菌區),中間是各種操作區域,按照污染風險由低到高排列。
以下是生技研發實驗室常見的八大功能分區。不是每間實驗室都需要全部八個——小型生技公司可能把某些功能合併在同一個空間,大型研究機構可能每個分區還會再細分。重點是分區的邏輯要對,實際的空間配置可以依規模和需求調整。

細胞培養室
細胞培養室是多數生技研發實驗室的核心空間,也是對環境條件要求最高的區域。這個空間的設計要同時滿足兩個有時候互相矛盾的需求:無菌(保護細胞不被污染)和生物安全(保護操作人員不被感染)。
設備配置的基本組合是 Class II BSC + CO₂ 培養箱 + 倒立式顯微鏡。BSC 提供無菌操作環境和人員防護,CO₂ 培養箱提供 37°C、5% CO₂、飽和濕度的細胞生長條件,倒立式顯微鏡用於日常觀察細胞生長狀態。
空間規劃上,幾個容易被忽略的細節:
- CO₂ 供氣:培養箱需要穩定的 CO₂ 供應。1–2 台培養箱用單鋼瓶就能應付,但如果有 4 台以上,建議用鋼瓶組搭配自動切換器,避免半夜鋼瓶用完影響培養。鋼瓶的放置位置和管路走向要在規劃階段就決定
- 人源細胞株 vs 非人源細胞株的分區:如果同時操作人源細胞(HeLa、293T 等)和非人源細胞(CHO、Vero 等),理想做法是分室操作。人源細胞株通常應視為潛在感染性材料,採 BSL-2 操作原則,但實際風險仍需依細胞來源、檢測資料、基因改造與 IBC/生安規範確認。非人源細胞株不一定都低風險——若涉及病毒、腫瘤來源或基因改造,也需另行風險評估。分不了室的情況下,至少用不同的 BSC、不同的培養箱,並建立明確的操作 SOP 和時間區隔
- 溫濕度控制:細胞培養室的環境溫度建議維持在 20–25°C,相對濕度 40–60%。不是因為細胞需要(細胞在培養箱裡),而是因為這個範圍對 BSC 的氣流穩定性和操作人員的舒適度都比較好
- 地坪與牆面:建議使用無縫、易清潔的材質,方便定期消毒。接縫處容易藏菌,對培養室來說是長期隱患
微生物操作區
微生物操作區和細胞培養室在設備上有重疊——都需要 BSC、都需要培養箱——但操作對象和風險特性不同,建議在空間上做分隔。
微生物培養(細菌、真菌)和哺乳動物細胞培養混在同一個空間,交叉污染的風險會顯著增加。微生物的生長速度遠快於哺乳動物細胞,一旦細菌或真菌進入細胞培養環境,往往整批培養毀掉。反過來,某些細胞實驗用的抗生素殘留也可能影響微生物培養的結果。
微生物區的設備配置通常包括 BSC、微生物培養箱(不需要 CO₂,但可能需要特定溫度範圍)、菌落計數器、以及就近的高壓滅菌鍋。如果涉及厭氧菌培養,還需要厭氧培養系統。
空間分隔的方式可以從「獨立房間 + 獨立空調」(理想做法)到「同一大空間但物理隔開 + 不同 BSC + 嚴格 SOP」(有限空間的折衷做法),依預算和規模決定。是否需要獨立空調,則應依操作微生物種類、風險等級、污染控制需求與 HVAC 可行性評估。
分子生物/基因工程區
分子生物學和基因工程操作——核酸萃取、PCR、電泳、轉染、基因編輯——對空間規劃最主要的要求是避免核酸交叉污染。
PCR 操作如果沒有做好區域分隔,擴增產物的微量殘留就可能造成假陽性結果。標準做法是至少分成「前 PCR 區」(試劑配製、樣品處理)和「後 PCR 區」(擴增、電泳、分析),兩區的耗材、微量吸管、實驗衣不互通。如果空間允許,加上獨立的「模板添加區」會更理想。
分子生物實驗室的設備空間需求包括 PCR 操作台(或專用的 PCR 操作台)、電泳系統、凝膠影像系統、即時定量 PCR 儀(qPCR)等。qPCR 儀如果數量多,發熱量和供電需求都要預留。
如果涉及基因重組實驗(例如慢病毒載體包裝、CRISPR),空間設計還要符合《基因重組實驗守則》的要求,通常需要在 BSL-2 條件下操作,並經 IBC 審查核可。
分析儀器區
生技研發實驗室常用的分析儀器——流式細胞儀、共軛焦顯微鏡、即時定量 PCR 儀、分光光度計、微量盤讀取儀——對環境的需求各有不同,但有幾個共通原則:
- 防震:流式細胞儀和共軛焦顯微鏡對振動敏感,建議放在低樓層或有防震處理的區域
- 溫控:精密光學儀器對溫度波動敏感,房間溫度建議維持在 20–25°C,日變化量 ±2°C 以內
- 獨立電力:高階儀器建議使用獨立迴路供電,避免與大功率設備(滅菌鍋、烘箱)共用迴路造成電壓波動
如果是多個研究團隊共用的儀器中心(core facility),空間規劃還要考慮預約管理的動線——操作者帶樣品進來、操作完帶數據出去,不需要穿過其他人的實驗操作區域。
試劑配製/前處理區
培養基配製、試劑分裝、樣品前處理的工作空間。這個區域通常不需要 BSC,但如果配製過程涉及化學溶劑(例如 DMSO、甲醛固定液),需要配置排煙櫃。
空間需求包括:實驗桌面、天平(配製培養基用)、pH 計、攪拌加熱器、純水系統、以及足夠的試劑儲存空間。如果培養基需要過濾滅菌(0.22 μm),過濾系統也要在這裡配置。
這個區域在潔污梯度上屬於「中間地帶」——比細胞培養室的潔淨要求低,但比一般化學前處理區乾淨。配製好的培養基要能「乾淨地」送進培養室,不需要穿過污染風險較高的區域。
清洗滅菌區
清洗滅菌區是生技研發實驗室裡「最不起眼但最容易出問題」的空間。這個區域同時處理污染物進入、滅菌處理、清洗乾燥與乾淨物品回流,所以要清楚區分待滅菌/污染側與已滅菌/乾淨側,避免乾淨物品與污染廢棄物交叉。
設備配置通常包括高壓滅菌鍋、超音波清洗機、烘箱(乾燥用)、以及足夠的不鏽鋼工作檯面。高壓滅菌鍋是這個區域的主角——它的容量選型(依每日操作量決定)、水電需求(三相電力、蒸氣或自帶加熱)、以及排水排汽的管路配置,都需要在規劃階段就確定。
動線設計上,清洗滅菌區的位置應該讓「髒東西進、乾淨東西出」的路徑不交叉。理想做法是設計成「進汙出淨」的穿越式配置——污染物從實驗區側進入,滅菌/清洗完成後從乾淨側出去。如果空間有限無法做穿越式,至少應透過標示、工作檯分區、暫存容器與操作順序,明確區分「待處理物」和「已處理物」。
實務觀察:高壓滅菌鍋的散熱量和水蒸氣釋放量常被低估。一台中型滅菌鍋運轉時的散熱量相當可觀,如果清洗滅菌區的通風沒有做好,夏天室溫可以飆到 35°C 以上,不只操作人員受不了,也會影響旁邊空間的溫度穩定性。規劃階段就要把滅菌鍋的散熱納入空調負載計算。
冷鏈儲存區
生技研發實驗室的冷鏈儲存需求通常涵蓋四個溫層:
- 4°C 冰箱:試劑、培養基、酵素的日常儲存
- -20°C 冷凍櫃:抗體、引子(primer)、部分試劑的中期儲存
- -80°C 超低溫冷凍櫃:細胞株暫存、蛋白質樣品、核酸樣品
- 液態氮儲存:長期細胞庫(cell bank)的保存
冷鏈儲存區的規劃要注意三件事:
散熱:-80°C 冷凍櫃和多台冰箱集中放置時,散熱量非常可觀。這個區域需要獨立或加強的通風排熱,否則環境溫度過高會導致冷凍櫃壓縮機負載過大、耗電增加、壽命縮短。
UPS 備援:-80°C 冷凍櫃和血庫冰箱建議接 UPS 或緊急電力,避免停電導致樣品損失。液態氮儲存本身不需要電力(被動式儲存),但如果用的是主動式液氮補充系統,供液管路和監控系統也需要備援電力。
液態氮安全:液態氮儲存區需要考慮氧氣濃度監測。液態氮蒸發會排擠空間中的氧氣,在通風不良的小空間裡有窒息風險。這個區域建議安裝低氧警報器,並確保通風換氣量足夠。
辦公/資料/輔助區
包括數據分析工作區、文獻查閱空間、更衣室、物料暫存區、以及人員休息區。這些空間在潔污梯度上屬於「最乾淨」或「非實驗」的區域,規劃上的重點是:
- 更衣區的位置應該在實驗區入口處,作為人員從一般區進入實驗區的緩衝
- 辦公區與實驗區物理分隔,避免在辦公區域穿實驗衣、戴手套(這是 BSL-2 的基本要求)
- 物料暫存區要考慮乾冰、試劑包裹的收貨動線
選型建議:規劃生技 R&D 實驗室的分區時,建議先把「細胞培養室」和「清洗滅菌區」的相對位置定下來——這兩個空間的關係是整個動線設計的錨點。培養用品要能「乾淨地進、污染地出」,而不是所有東西都走同一條路。把這個關係定好,其他分區的位置就會比較容易安排。
四、人員淨化動線與廢棄物分流
生技研發實驗室的動線設計,和化學實驗室或品管實驗室有一個很大的差異:你不只要管「人怎麼走」,還要管「乾淨的東西怎麼進來」和「髒的東西怎麼出去」——而且這三條路徑不應該交叉。
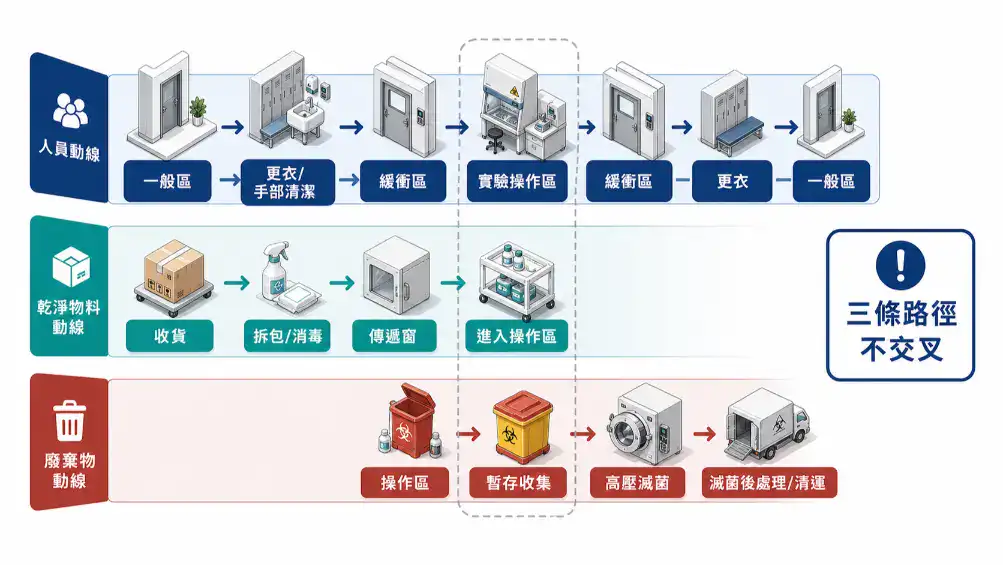
人員動線——從一般區到操作區的淨化梯度
BSL-2 實驗室的人員進出動線應該有一個「緩衝帶」,讓人員在進入操作區域前完成必要的防護準備。最基本的流程是:
一般區 → 更衣(穿實驗衣/戴手套) → 手部清潔 → 進入實驗操作區
這個流程看起來簡單,但空間上需要一個實際可用的更衣/緩衝區域。很多小型生技公司在規劃時把更衣區壓縮到一個小角落,結果人員更衣的時候轉身都困難,久了大家就懶得按照 SOP 走——防護措施形同虛設。
更衣區的空間建議至少能容納:掛實驗衣的衣架或衣櫃、放手套和個人防護裝備的收納、一個免手動式洗手槽。如果是 BSL-2,更衣區的門最好設計成不會同時和實驗區及一般區的門同時打開(不需要像 BSL-3 那樣做雙門互鎖,但至少有物理上的分隔)。
物料動線——乾淨物料和生物廢棄物不走同一條路
物料動線要處理的是兩個方向的流動:
進入方向:乾淨的試劑、耗材、培養基從外部進入實驗室。理想的路徑是:收貨區 → 物料暫存 → 拆包/消毒 → 進入使用區域。如果有傳遞箱(pass box),可以讓物料在進入潔淨度要求較高的區域前先做表面消毒。
離開方向:使用過的培養器具、含生物材料的廢棄物從實驗室移出。生物廢棄物的路徑應該是:操作區 → 暫存/收集 → 高壓滅菌 → 滅菌後作為一般廢棄物處理或委外清運。
這兩條路徑不交叉,是生技 R&D 實驗室動線設計的底線。實際操作上,最常出問題的環節是高壓滅菌鍋的位置。如果滅菌鍋放在實驗室的「另一頭」,操作人員就得捧著一袋生物廢棄物穿過半個實驗室才能去滅菌——這段路徑上經過的每一個區域都是潛在的污染風險。
廢棄物分類與暫存
生技研發實驗室的廢棄物通常分成三類:
- 感染性或具生物風險廢棄物:接觸過 RG2 以上病原體、人源細胞、病毒載體或其他具生物風險材料的培養器具、培養液與耗材,應依生物風險、廢棄物類型與 SOP 進行高壓滅菌、化學滅活或合規委外處理
- 基因改造生物體廢棄物:基因重組實驗產生的菌液、培養物、病毒載體相關耗材等,應依 IBC 核准條件與機構 SOP 進行滅活或其他合規處理
- 一般實驗廢棄物:未接觸感染性材料的一般耗材、包裝材料
每類廢棄物需要獨立的收集容器和暫存空間。感染性廢棄物的收集容器應該有明確的生物危害標示,放在操作區域可及之處。暫存區的大小依實驗室的操作量和滅菌鍋的處理頻率而定——如果每天跑一次滅菌鍋,暫存空間可以小一些;如果一週只跑一到兩次,暫存空間就要相應加大。
三流分離在有限空間裡的折衷
理想的三流分離——人流、物流、廢棄物流各有獨立的動線——在大型研究機構或新建案裡比較容易做到。但多數生技公司,特別是新創公司或中小型研究單位,空間有限,完美的三流分離不太現實。
在有限空間裡,建議守住的最低限度是:
- 廢棄物的搬運路徑不回穿細胞培養區
- 人員進出實驗區有緩衝空間(即使只是一個小前室)
- 乾淨物料的進入和生物廢棄物的移出在時間或空間上做區隔
這三點如果做到,即使空間不大,動線的安全性和合理性也能維持在可接受的範圍。
五、環境控制與空調壓差設計
生技研發實驗室的環境控制,比一般辦公空間或化學實驗室多了一個維度:壓差。你不只要管溫度和濕度,還要管空氣往哪個方向流。
壓差控制——定向氣流的設計邏輯
前面在 BSL 分級那一章已經提過,BSL-2 的壓差設計是「定向氣流」——空氣從低風險區流向高風險區。具體到生技 R&D 實驗室,壓差梯度的層級安排通常是:
走廊(微正壓或常壓) → 一般實驗區(常壓或微負壓) → BSC 操作區/細胞培養室(微負壓) → 清洗滅菌區(負壓)
這個梯度確保:如果門被打開或密封不完美,空氣會「往裡吸」而不是「往外漏」。對於操作感染性生物材料的區域,這個方向至關重要。
壓差的數值不需要做得很大。若需負壓,可先以小幅壓差作為設計起點,實際數值需由 HVAC 設計、風量平衡與現場驗證確認。壓差太大反而會造成開門困難、門會自動被吸住或彈開(取決於開門方向),操作人員的體驗會很差。
不過,這裡有一個生技 R&D 實驗室獨有的設計矛盾:細胞培養室從「生物安全」的角度需要負壓(防止生物材料洩漏),但從「無菌培養」的角度又希望正壓(防止外界微生物進入)。怎麼取捨?
細胞培養室的壓差應依生物安全風險與樣品保護需求決定。一般 BSL-2 R&D 場景,可透過 Class II BSC 提供操作層級的人員、產品與環境防護——BSC 內部本身就是高潔淨度的操作環境(通過 HEPA 過濾的下吹氣流),培養箱也是密閉系統。所以房間壓差的設計有一定彈性,不一定要一概套用負壓。但若涉及 GTP、細胞治療產品製備或更高潔淨要求,則需回到潔淨室與製程規範另行設計壓差與氣流,不宜直接套用一般 BSL-2 R&D 的邏輯。
溫濕度與空氣品質
生技研發實驗室各區域的溫濕度需求不同,但大致可以分兩類:
一般實驗區域(包括細胞培養室、微生物區、分子生物區):溫度 20–25°C,相對濕度 40–60%。這個範圍對 BSC 的氣流穩定性最好,也讓操作人員穿著實驗衣工作不會太悶。
儀器分析區域:溫度穩定性比絕對溫度更重要。精密光學儀器(流式細胞儀、共軛焦顯微鏡)建議日溫差控制在 ±2°C 以內。
空調系統的獨立性是一個常被忽略的問題。生技研發實驗區域的空調建議和辦公區域、公共區域分開,原因有三:操作時段可能不同(有些培養作業需要在非上班時段進行,空調不能跟著辦公區一起關);壓差控制需要獨立調節;以及生物操作區的換氣量通常比辦公區高,混在一起會增加空調系統的控制複雜度。
CO₂ 供氣系統的選擇
CO₂ 培養箱的 CO₂ 供氣是生技研發實驗室獨有的需求,供氣方式的選擇取決於培養箱的數量:
- 1–2 台培養箱:單鋼瓶供氣即可。CO₂ 鋼瓶的使用時間會受培養箱容量、開門頻率、箱體密封性與管路狀況影響很大,建議以實際消耗紀錄估算更換頻率
- 3–5 台培養箱:建議使用鋼瓶組搭配自動切換器。當 A 鋼瓶用完時自動切換到 B 鋼瓶,避免 CO₂ 供應中斷影響細胞培養
- 6 台以上:可考慮中央供氣系統(CO₂ 液態儲槽 + 管路配送),長期運轉成本較低,也省去頻繁換鋼瓶的人力
鋼瓶的放置位置和管路走向需要在規劃階段決定。CO₂ 鋼瓶建議放在通風良好的位置,避免放在密閉空間——雖然 CO₂ 不可燃不助燃,但大量洩漏時有窒息風險。管路材質應依氣體純度、壓力、設備接口與洩漏風險選擇,常見選項包含不鏽鋼、銅管或符合氣體用途的專用管材,管路應盡量簡潔並設置適當固定與洩漏檢查機制。
六、設備配置與選型重點
生技研發實驗室的設備清單會隨著研究方向和專案階段變動——這是 R&D 場景和 QC/臨床實驗室最大的差異之一。QC 實驗室的設備組合相對固定(HPLC、天平、溶離試驗機⋯⋯),但 R&D 實驗室可能今年做細胞培養,明年增加基因編輯,後年引進流式細胞儀。
所以設備配置的規劃原則不是「把每台設備的位置釘死」,而是「把水電氣管路的預留和承重散熱的彈性做好」。設備會換,管路預留改不了。
以下按設備類別,點出生技 R&D 場景的選型考量。
生物安全櫃——從「要不要」到「要哪一型」
在 BSL-2 實驗室裡,涉及感染性材料或氣膠風險的操作都需要 BSC,它不只是「有比較好」的選配。問題是要選哪一型。
對多數生技研發操作(細胞培養、微生物接種、核酸萃取等),Class II A2 型 BSC 是相當常見的選擇,能在多數非揮發性化學品、非放射性物質的生物操作中提供人員防護、產品防護和環境防護。
什麼時候需要考慮 A2 以外的選擇?
- 如果操作過程涉及揮發性化學品或放射性物質——例如使用 ³H 標記的核苷酸做示蹤實驗——需要評估是否改用 B2(全排式)或 C1(可切換排氣模式)。典型 Class II A2 BSC 會有部分氣流經 HEPA 過濾後再循環,因此不適合大量或持續使用揮發性有毒化學品。若操作涉及此類物質,應評估 B2、C1 或其他專用控制設備
- 如果研究涉及高風險病原體(BSL-3),Class II B2 或 Class III BSC 是比較常見的配置
BSC 和排氣系統的搭配也是規劃階段就要確認的事。A2 型 BSC 可以透過櫃頂集氣罩(thimble connection)連接到排氣系統,也可以不接(直接排到室內,前提是室內有足夠的換氣量)。B2 型則必須硬管直連排氣系統,而且對排氣系統的靜壓和風量有明確要求——這一點在 BSC 選購檢查清單裡有詳細說明,很多採購踩坑都踩在這裡。
CO₂ 培養箱——不只是溫度和 CO₂
CO₂ 培養箱是細胞培養的核心設備,選型時除了基本的溫度和 CO₂ 控制,還有幾個生技 R&D 場景比較在意的面向:
氣套式 vs 水套式:氣套式加熱速度快、恢復時間短,適合開門頻率高的研究實驗室。水套式保溫性好,斷電後溫度維持時間長,但加熱恢復較慢。對於每天開門多次的 R&D 場景,氣套式因回溫速度快而常被採用。是否配置 UPS 或緊急電源,則應依細胞樣品重要性、斷電風險與設備負載決定。
低氧培養(Hypoxia):如果你的研究涉及幹細胞、腫瘤微環境、缺氧誘導因子等方向,可能需要能控制 O₂ 濃度的培養箱(將 O₂ 降到 1–5%)。低氧培養箱需要額外的 N₂ 供氣,管路和鋼瓶的配置要一併規劃。
污染控制方式:高溫乾熱滅菌(180°C 或 200°C)、紫外線照射、H₂O₂ 蒸氣——不同品牌採用不同的箱內消毒機制。高溫乾熱最徹底,但每次執行要花 10 小時以上,期間培養箱無法使用。對於培養箱數量有限的小型實驗室,這個時間成本需要考慮。
超低溫冷凍與液態氮儲存
-80°C 超低溫冷凍櫃用於細胞株暫存、蛋白質樣品和核酸樣品的中期保存。液態氮儲存用於長期細胞庫(master cell bank / working cell bank)的保存。
設備選型之外,空間規劃要注意:
- -80°C 冷凍櫃的散熱量大。一台立式 -80°C 冷凍櫃的散熱量大約等於一台小型電暖器,如果放在通風不好的角落,周圍環境溫度可以升高到影響冷凍櫃效能的程度
- 液態氮區域需要低氧警報和通風。小空間放多台液態氮桶,蒸發的氮氣會排擠氧氣,這不是理論上的風險,是實際發生過事故的場景
- -80°C 冷凍櫃應納入緊急供電、溫度監測、遠端警報與樣品轉移 SOP。是否配置 UPS,需依冷凍櫃啟動電流、持續負載與備援策略評估——對多數場景而言,緊急電源、備援冷凍櫃、溫度警報與清楚的樣品轉移流程,往往比單純配置 UPS 更務實。停電後溫度上升速度會受冷凍櫃型號、裝載量、門封狀態和環境溫度影響,規劃時應依實際設備進行風險評估
清洗與滅菌設備
高壓滅菌鍋的容量選型需要和日常操作量匹配。生技 R&D 實驗室每天產生的需滅菌廢棄物量,主要取決於操作的種類和頻率。一般來說:
- 小型實驗室(2–3 人,日常細胞培養和分子生物操作):50–75 L 的桌上型或立式滅菌鍋
- 中型實驗室(5–10 人,多種操作同時進行):75–120 L 立式
- 大型研究單位或多個實驗室共用:150 L 以上,考慮雙扉穿牆式
滅菌鍋的水電需求常被低估。中大型滅菌鍋通常需要三相電力、給水和排水管路。電力容量、給水壓力和排水管徑,規劃階段就要確認。
超音波清洗機用於玻璃器皿的精密清洗,在反覆使用玻璃移液管、燒瓶的實驗室裡是必需品。現在越來越多實驗室改用拋棄式塑膠耗材,超音波清洗機的需求可能沒有以前那麼高,但如果有玻璃器皿清洗需求,配一台不大的桌上型通常就夠了。
七、法規框架與生物安全管理
生技研發實驗室的法規框架和化學實驗室不同——化學實驗室主要面對的是毒化物管理法規和職安法規,生技 R&D 實驗室面對的是一套以「生物安全」為中心的法規體系。了解這套體系的架構,對規劃階段的設計決策有直接影響。
台灣生物安全法規的基本架構
台灣的生物安全法規可以分成幾個層級:
感染性生物材料管理辦法(衛福部疾管署):這是最上位的管理法規,規範感染性生物材料的持有、使用、保存、銷毀和傳送。如果你的實驗室操作 RG2 以上的病原體,這個辦法的要求直接影響實驗室的設計(BSL 等級、門禁、廢棄物處理等)。
基因重組實驗守則(國科會/各機構 IBC):如果涉及基因重組實驗(包括基因轉殖、基因編輯、病毒載體包裝等),須依守則向所屬機構的生物安全委員會(IBC)申請核可。IBC 會審查實驗內容、實驗室設施條件、操作人員資格和緊急應變計畫。
實驗室生物安全技術規範及指引(疾管署):疾管署網站設有「實驗室生物安全技術規範及指引」專區,包含多份規範、指引、緊急應變與病原體相關文件。其中提供 BSL-1 到 BSL-4 實驗室的設施規格、操作規範和管理要求的說明,是各機構生安委員會在審查和稽核時的主要參考依據之一。
GTP(人體細胞組織優良操作規範)(衛福部):適用於細胞治療產品的製備場所。如果你的研發方向涉及自體或異體細胞治療產品的製備,空間設計需要符合 GTP 的潔淨度和操作規範要求。
IBC 生物安全委員會的角色
IBC 在生技研發實驗室的規劃中扮演一個常被低估的角色。很多人以為 IBC 只管「實驗核准」,但 IBC 的審查範圍包含實驗室設施條件——也就是說,你的實驗室硬體設計如果不符合 IBC 的要求,實驗計畫可能無法獲得核可。
對新建或改建的生技研發實驗室,建議在規劃階段就把預計的研究內容和 BSL 等級告知 IBC(或所屬機構的環安衛單位),讓他們在設計階段就能提供意見。等到空間蓋好了再去送審,如果 IBC 認為設施條件不符合要求,改起來的成本和時間會很可觀。
企業端如果沒有自己的 IBC(例如小型生技新創),可以委託外部機構(如學術單位或法人機構)的 IBC 協助審查,但實驗室的硬體條件仍然需要符合相應的 BSL 要求。
年度查核與維護
BSL-2 實驗室啟用之後,有幾項定期維護和查核的工作需要持續執行:
- BSC 定期認證:BSC 通常需定期認證檢測,移機、更換 HEPA、維修或氣流異常後也應重新確認性能。檢測頻率與項目依機構規範、疾管署指引及適用標準確認。詳細的檢測項目和常見不合格原因,可以參考 BSC 年度認證檢測指南
- 高壓滅菌鍋效果確認:滅菌鍋應依用途與風險定期執行效果確認,包括物理參數記錄、化學指示劑與生物指示劑。測試頻率依機構 SOP、廢棄物風險、使用頻率與主管機關要求決定
- 生安演練:BSL-2 實驗室應每年辦理生物安全模擬應變演練
- 人員訓練:操作人員需定期完成生物安全訓練時數
這些年度維護工作的空間需求——BSC 認證時需要操作空間、滅菌鍋確效時需要取樣和判讀的空間——在規劃階段不會佔太多面積,但至少要確保設備周圍有足夠的工作空間讓認證人員操作。
八、生技醫藥研發實驗室的規劃流程
生技研發實驗室的規劃流程和一般實驗室的框架類似(可參考實驗室規劃設計完整手冊),但有幾個生技 R&D 特有的環節需要特別注意。以下是我們建議的七步驟流程:
步驟一:需求訪談——從研究方向定義空間需求
規劃的第一步不是畫平面圖,而是釐清「這間實驗室要做什麼」。對生技研發實驗室而言,需要確認的事項包括:
- 研究方向和操作的生物材料類型(人源細胞株?RG2 病原體?基因重組?病毒載體?)
- 目前和未來 3–5 年預計的研究規模(幾個研究團隊?幾個人同時操作?)
- 是否涉及 GTP 或臨床試驗材料的製備
- 既有空間的條件限制(樓層承重、天花板高度、既有管路位置)
步驟二:法規盤點——確認 BSL 等級和審查要求
根據需求訪談的結果,確認實驗室需要達到的 BSL 等級,並盤點對應的法規要求:感染性生物材料管理辦法、基因重組實驗守則、GTP(如適用)。這一步建議同步知會 IBC 或環安衛單位。
步驟三:分區與動線設計
根據 BSL 等級和操作類型,設計功能分區和動線。這一步要處理的問題包括:潔污梯度怎麼排列、細胞培養室和清洗滅菌區的相對位置、人員淨化動線、廢棄物分流路徑。
步驟四:設備清單與管路預留
列出現階段需要的設備清單,同時預留未來可能新增設備的水電氣管路。生技 R&D 的設備組合會隨專案變動,所以管路預留比設備定位更重要。BSC 的排氣接口、培養箱的 CO₂ 管路、滅菌鍋的蒸氣/排水、-80°C 冷凍櫃的散熱空間和電力,都是這一步要確認的。
步驟五:環境控制設計
空調壓差、溫濕度控制、CO₂ 供氣系統的設計。這一步需要和空調工程團隊密切配合,確保壓差梯度、換氣量和控制方式都符合 BSL 等級的要求。
步驟六:施工與系統整合
施工階段的重點是確保各系統(空調、電力、給排水、氣體管路、門禁)的整合不出問題。生技研發實驗室的系統整合比一般辦公裝修複雜,建議由有實驗室建置經驗的團隊統籌施工,避免各工種各做各的導致系統衝突。
步驟七:驗收與啟用
驗收的重點項目包括:
- 空調壓差確認(各區域的壓差值是否符合設計要求)
- BSC 安裝後認證(安裝位置氣流條件、HEPA 洩漏測試、風速測試)
- 高壓滅菌鍋功能驗證和生物確效
- 門禁系統測試
- IBC 或環安衛單位的實地查核
- 人員培訓和 SOP 建立
IBC 實地查核通常是 BSL-2 實驗室啟用前的最後一關。查核項目涵蓋設施硬體、管理制度、人員資格和緊急應變計畫。建議在送審前先做一次內部自評,確認硬體和文件都到位。
常見問題 FAQ
Q1:生技研發實驗室的規劃時程大概要多久?
從需求訪談到正式啟用,BSL-2 等級的生技研發實驗室常見可能落在數月至半年以上,實際時程取決於面積、既有空間條件、HVAC 改造幅度、設備交期、IBC/生安審查與驗收項目。如果是既有空間改建,施工時程通常比新建短,但可能需要額外處理既有管路拆改的問題。涉及 GTP、潔淨室或更高等級的空間,時程通常需要再拉長。
Q2:BSL-1 和 BSL-2 實驗室的建置成本差距大嗎?
差距主要來自空調系統(BSL-2 需要定向氣流和壓差控制)、BSC、高壓滅菌鍋、門禁、清潔材質和驗證測試。同樣面積下,BSL-2 的建置費用通常會明顯高於 BSL-1,但差距不能只用固定百分比估算,實際金額取決於既有空間條件、HVAC 改造幅度、設備規格和審查要求。
Q3:細胞培養室需要做到無塵室等級嗎?
多數 BSL-2 R&D 場景的細胞培養室不需要做到正式的無塵室等級(如 ISO Class 7 或 Class 5)。關鍵操作在 BSC 內完成,BSC 內部本身就提供高潔淨度的操作環境;培養箱也是密閉系統。所以培養室的背景環境不需要達到無塵室等級,但建議維持良好的清潔狀態、使用無縫易清潔的地坪和牆面材質、控制人員進出和非必要物品。不過,若涉及 GTP、臨床用細胞製備或細胞治療產品,就不能用一般 R&D 標準判斷,應依製程特性、GTP 要求與主管機關審查確認背景潔淨度與壓差。
Q4:生技研發實驗室可以和品管實驗室共用空間嗎?
可以共用部分公共空間(例如清洗區、儲存區、辦公區),但操作區域建議分開。兩者的操作對象、法規要求和動線邏輯不同:R&D 以生物安全風險管理為主軸,QC 以樣品追溯和數據完整性為主軸。混在一起操作容易造成管理上的混亂。如果生技公司同時有 R&D 和 QC 需求,比較常見的做法是在同一棟建築內設計為獨立的區域,共用基礎設施(空調主機、電力系統、純水系統)但操作空間和動線各自獨立。
Q5:外泌體或基因治療研究的實驗室有什麼特殊需求?
外泌體研究的特殊需求主要在超速離心機(佔地大、振動大、需要防震基座和獨立電力)和超低溫儲存(外泌體樣品通常保存在 -80°C)。如果涉及外泌體的分析和定量,可能需要奈米粒子追蹤分析儀(NTA)等精密儀器,對防震和溫控有要求。
基因治療研究如果涉及病毒載體的包裝和生產(例如 AAV、慢病毒),操作通常需要在 BSL-2 條件下、Class II BSC 內進行,並且須經 IBC 核可。病毒載體操作的廢棄物處理要求比一般細胞培養更嚴格——所有接觸過病毒的培養器具和液體都必須經過滅菌處理。
Q6:既有空間改建成 BSL-2 實驗室,最常遇到什麼問題?
改建最常遇到的三個問題:
第一是天花板空間不足。BSL-2 需要定向氣流的空調系統,風管需要在天花板內走管。很多既有空間的天花板高度本來就有限,加上風管之後可用高度不夠(BSC 的櫃頂到天花板建議保留至少 30 cm,50 cm 以上更理想)。
第二是排水和給水管路改線困難。高壓滅菌鍋需要給水和排水,BSL-2 的洗手槽最好是免手動式——這些都需要管路到位。既有空間的管路位置不一定在你需要的地方,改管的成本和工期常常超出預期。
第三是空調系統容量不足。既有建築的空調主機可能沒有預留足夠的冷量和風量給 BSL-2 實驗室的壓差控制和換氣需求。這個問題如果到施工階段才發現,可能需要增設獨立空調系統,費用和時程都會大幅增加。
Q7:怎麼選擇生技研發實驗室的規劃廠商?
選擇規劃廠商時,建議確認幾個面向:
- 有 BSL-2 實驗室的實際建置經驗:BSL-2 的空調壓差控制、動線設計和 BSC 排氣整合都需要經驗。沒有做過 BSL-2 的廠商,很容易在這些環節踩坑
- 能整合設備和空間:生技研發實驗室的設備(BSC、培養箱、滅菌鍋、冷凍櫃)和空間(空調、電力、管路)需要整合規劃,不是分開發包就能搞定的
- 了解法規框架:廠商需要理解 BSL 分級的硬體要求、IBC 查核的標準,才能在設計階段就把合規的需求做進去
- 提供驗收和後續服務:BSC 認證、滅菌鍋確效、空調壓差測試——這些啟用後的服務,最好在規劃階段就確認廠商是否能提供或協調
相關產品分類
延伸閱讀
- 實驗室規劃設計完整手冊
- 生物安全櫃完整指南:分級、選型、安裝與維護
- 生物安全櫃 vs. 無菌操作台:差異、選擇與常見誤用
- BSC 選購檢查清單:採購前必須確認的 10 件事
- CO₂ 培養箱完整指南
- -80°C 超低溫冷凍櫃完整指南
- 實驗室冰箱與冷凍櫃選購比較指南
- GMP 工廠 QC 品管實驗室規劃指南
- 實驗室通風與排氣系統設計指南
- HEPA 與 ULPA 濾網完整解析
- 超音波清洗機完整指南
原拓科技在實驗室建置服務和完整解決方案中,整合了空間規劃、設備選型和後續維護認證的一站式服務。如果你正在規劃生技研發實驗室,歡迎與我們聊聊你的需求。
